Алюмо-калиевые квасцы
Cтраница 3
Некоторые соли алюминия применяют в медицине для лечения кожных заболеваний: KA1 ( SO4) 2 12Н2О - алюмо-калиевые квасцы: ( СН3СОО) 3А1 - ацетат алюминия. Оксид алюминия А ] 2О3 используется в качестве адсорбента в хроматографии. Хлорид алюминия А1С13 применяется в качестве катализатора в органической химии. Сульфат алюминия A12 ( SO4) 3 18H2O используется для очистки воды. [31]
Кроме того, в производстве обычно применяют не уксуснокислые алюминий и кальций, а более доступные сернокислый алюминий ( или алюмо-калиевые квасцы) и хлористый кальций. [32]
Для этого в емкость 10 заливают 40 л горячей воды, включают перемешивающее устройство и затем порциями загружают расчетное количество алюмо-калиевых квасцов. Если раствор приготовлен ранее, необходимо лишь довести его до заданной температуры. Термостаты 3 и 14 должны быть включены и разогреты до заданной температуры заблаговременно. [33]
Сущность определения нитратов ионометрическим методом состоит в извлечении их из анализируемого материала 1 % - ным раствором сульфата калия - алюминия ( алюмо-калиевых квасцов) и последующем измерении концентрации нитрат-ионов в полученной вытяжке ионоселективным электродом. Метод применим для анализа сырого растительного сырья, в которое не добавляют хлориды. [34]
Раствор алюминия ( раствор А), содержащий 1 мг алюминия в 1 мл, готовят следующим образом: 17 584 г невыветрившихся алюмо-калиевых квасцов ( KAl ( SO4) 2 12H2O) высыпают в литровую мерную колбу, приливают дистиллированной воды, добавляют 1 мл перегнанной азотной кислоты, перемешивают до растворения соли и доливают дистиллированной водой до метки. Раствор В содержит 0 1 мкг алюминия в 1 мл. [35]
Остаток смыть в стакан 5 - 6 мл азотной кислоты ( разбавленной 1: 3) и ополоснуть воронку водой; прибавить 4 - 5 мл раствора алюмо-калиевых квасцов, нагреть до кипения, прибавить водного аммиака до сильного запаха и фильтровать через бумажный фильтр. [36]
Из алюминиевых солей по тем же причинам пригодны сернокислые и азотнокислые соли, а также алюмо-аммонийные квасцы. Алюмо-калиевые квасцы для производства синего кобальта менее пригодны, так как они полностью разлагаются лишь при более высокой температуре. [37]
Таковы алюмо-калиевые квасцы KA1 ( SO4) 2 - 12H2O, хромово-калиевые квасцы KCr ( SO4) 2 - 12H2O, соль Мора ( NH4) 2Fe ( SO4) 2 - 6H2O, гексацианоферрат ( П) калия К4 [ Ре ( СМ) 6 ] ит. [38]
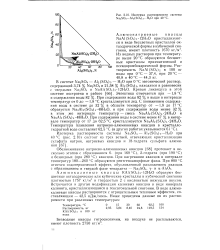 |
Изотерма растворимости системы Na2SO4 - A12 ( SO4 3 - Н2О при 40 С. [39] |
Встречается и другая модификация калиевых квасцов в виде минерала калинита, кристаллизующаяся в гексагональной сингонии. В воде алюмо-калиевые квасцы растворяются с отрицательным тепловым эффектом, составляющим - 42 5 кДж / моль. [40]
В продукте дегидратации гексагидрата хлорида кобальта ( II) релаксация решетки наиболее велика. Поскольку продукты дегидратации алюмо-калиевых квасцов имеют открытую структуру, то здесь подвижность сферических ионов, образующих решетку, значительна в присутствии паров воды, а степень рекристаллизации оказывается большой. [41]
Оценивая предварительно пригодность квасцов для разделения цезия, рубидия и калия в процессе фракционирования, надо учитывать способность различных квасцов к образованию ( вследствие изоморфизма) твердых растворов. Как уже отмечено, алюмоцезиевые и алюмо-калиевые квасцы твердых растворов не образуют. В связи с этим основная трудность при использовании квасцового метода заключается в разделении рубидия и цезия, рубидия и калия, но не цезия и калия. По данным [196, 197] для получения алюморубидиевых квасцов, свободных от калия, требуется от 12 до 22 перекристаллизации технического продукта. [42]
NaOH потенциометрически или по смешанному индикатору. Нейтрализованный раствор титруют раствором алюмо-калиевых квасцов потенциометрически или визуально до перехода окраски из зеленой в фиолетовую. [43]
При этом в осадок выделяются алюмо-калиевые квасцы, плохо растворимые при невысокой температуре. В маточном растворе после отделения кристаллов алюмо-калиевых квасцов остаются растворимые примеси - соединения железа и хлорид натрия. [44]
Страницы: 1 2 3