Кетелар
Cтраница 1
Кетелар [2] детально изучил структуру безводного хлористого алюминия после очистки его повторной сублимацией в высоком вакууме. [1]
Описывая молекулярные соединения, Кетелар [139] относил к ним многочисленную группу веществ, Б которых связывание осуществляется вандервааль-совскими силами, составляющими от / ю до / 2о части энергии большинства атомных или ионных связей и, следовательно, не могущими привести к образованию химических соединений с устойчивыми молекулами. Ниже приводится классификация этих соединений, предложенная Кетеларом. [2]
Метод измерения силы кислоты был использован Кетеларом [67] в 1951 г. В табл. 15 приведены некоторые примеры из группы замещенных ароматических диэтилфосфатов. Если отщепившийся фенол ХОН является сильной кислотой, то фосфат должен быть хорошим ингибитором. Как видно из данных табл. 15, эта зависимость носит лишь качественный характер. [3]
В случае применения уравнения ( 13) ( уравнение Кетелара [8]) на графике зависимости величин 1 / ( еа - ед) от I / CD получают прямую линию. Коэффициент экстинкции комплекса ( БОА) вычисляют из отрезка, отсекаемого этой линией на оси ординат, а величину / Сс - из этого отрезка и наклона прямой. Уравнение Бенеши - Гильдебранда [ уравнение ( 8) глава И ] [10], которое часто использовали при вычислении констант равновесия образования комплекса, можно получить из уравнения ( 13), приняв, что ед ничтожно мало по сравнению с еа или еод. [4]
Первыми из таких соединений являются этилсульфаты лантанидов Ьп ( С2Н55О4) з - 9Н2О, которые были изучены рентгенографически вначале Кетеларом [4] и позднее Фитцватером и Рундле [5], исследовавшими соединения празеодима, эрбия и иттрия. [5]
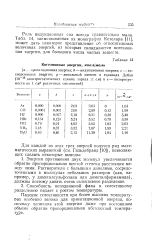 |
Когезионные энергии, ккал / моль. [6] |
Роль индукционных сил всегда сравнительно мала. Кетелара [11], может дать некоторое представление об относительных величинах энергий, из которых складывается когезион-ная энергия, для большого числа чистых веществ. [7]
В последнем случае для локализации связи требуется гораздо большая энергия, чем в первом, так как система ( XXX) обладает большей энергией. Койман и Кетелар нашли, что ал я образования структуры ( XXIX) требуется 29 ккал / моль, а для образования структуры ( XXX), по крайней мере, 55 ккал / моль. Значения энергий сопряжения в молекулах нафталина и бензола, применявшиеся в их расчетах, были позднее уточнены, но остается в силе вывод, что энергия необходимая для локализации двойной связи 2 - 3, настолько велика, что при нормальной химической реакции такая локализация невозможна, в то время как локализация ( или фиксирование) связи 1 - 2 с образованием структуры, предложенной Физером и другими, должна происходить легче, чем локализация любой связи в молекуле бензола. Однако общее распределение связей в молекуле нафталина соответствует описанию Полинга и др. Тем не менее было бы хорошо избегать термина подвижность двойных связей в качестве синонима понятия сопряжения в молекуле нафталина. Когда связь близка к двойной, достаточно малого количества энергии, чтобы она стала чисто двойной; если же она ближе к ординарной, то для ее превращения в двойную требуется энергия, значительно превышающая барьер химических реакций. [8]
Описывая молекулярные соединения, Кетелар [139] относил к ним многочисленную группу веществ, Б которых связывание осуществляется вандервааль-совскими силами, составляющими от / ю до / 2о части энергии большинства атомных или ионных связей и, следовательно, не могущими привести к образованию химических соединений с устойчивыми молекулами. Ниже приводится классификация этих соединений, предложенная Кетеларом. [9]
При изучении инфракрасных спектров твердых веществ широко используют методику приготовления прессованных таблеток с галогенидами щелочных металлов. Несколькими исследователями было отмечено, что интерпретацию спектров, полученных при использовании подобной методики, следует проводить с осторожностью. Например, Кетелар и др. [353] заметили, что v3 - частота колебаний иона [ HF2 ] -, довольно чувствительна к тому, какой из галогенидов щелочных металлов при этом используется и имеет значения 1599, 1570, 1527 и 1478 слгь в таблетках с NaBr, KC1, КВг и KI соответственно. С другой стороны, спектры NaHF2, KHF2 и NH4HF2, приготовленных в таблетках с КС1, одинаковы. [10]
Результаты измерения мономолекулярных констант скорости гидролиза и взаимодействия с ацетилхолинэстера-зой ( в сопоставимых условиях) показали, что логарифмы этих величин для исследованной серии соединений приближенно укладываются в линейную зависимость, причем, чем выше константа скорости гидролиза, тем выше и антихолинэстеразная активность. Такой характер зависимости, несомненно, связан с однотипным влиянием электрофильности радикала Аг на обе реакции. Для ароматических радикалов, исследованных Олдриджем и Девисоном, относительная электрофильность может быть количественно оценена величиной константы диссоциации соответствующего фенола Аг - ОН. При этом оказалось, что между силой кислоты Аг-ОН и константами скорости щелочного гидролиза и взаимодействия с холинэстеразами наблюдается определенная зависимость. Аналогичные результаты были получены Кетеларом [149] и другими авторами. [11]
Страницы: 1