Стерически затрудненный кетон
Cтраница 1
Стерически затрудненные кетоны восстанавливаются комплексными гидридами металлов главным образом в аксиальные спирты, если атака реагента с аксиальной стороны затруднена. [1]
Даже стерически затрудненные кетоны типа димезитилке-тона без труда восстанавливаются алюмогидридом лития. [2]
Для альдегидов и алифатических кетонов равновесие смещено вправо; следовательно, реакция вполне осуществима, кроме случаев таких стерически затрудненных кетонов, как диизопропилкетон. Однако кетоны типа ArCOR дают низкие выходы, а реакцию с АгСОАг провести не удается потому, что равновесие сильно сдвинуто влево. [3]
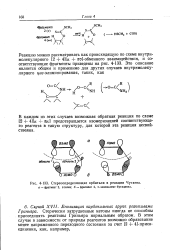 |
Стереоопределяющие орбитали в реакции Чугаева. а - фрагментЗ, этилен. б - фрагмент 4, it - эквивалент бутадиена. [4] |
Стерически затрудненные кетоны иногда не способны присоединять реактивы Гриньяра нормальным образом. [5]
Бартон установил, что для стереохимической оценки восстановления кетонов необходимо принимать во внимание конформации исходных соединений. Он классифицирует кетоны на два типа: на стерически затрудненные кетоны, в обычных условиях не реагирующие с реагентами на карбонильные группы, и на стерически незатрудненные, реагирующие с этими соединениями. [6]
Так как сложные эфиры менее реакционноспособны по отношению к реактивам Гриньяра или литнйорганическим соединениям чем кетоны, реакцию обычно не удается остановить иа стаднн образования кетона. Это можно сделать только в том случае, когда есть и сложный эфир, и металлоорганическое соединение содержат третичные алкильные группы, затрудняющие последующее взаимодействие стерически затрудненного кетона с трет. [7]
Восстановление циклических кетонов осуществляется с высокой степенью стереоселективности. При восстановлении кетогруппы сложных полициклических систем стереоселективность реакции зависит от пространственной доступности кетогруппы: действие алюмогидрида лития на сте-рически незатрудненные кетоны приводит к образованию преимущественно спиртов с экваториальной гидроксильной группой, а из стерически затрудненных кетонов в этой реакции образуются главным образом спирты с аксиальным положением гидроксила. [8]
Снятие защиты производится действием сильных кислот в среде ацетона. Легкость удаления защитной группы коррелирует с легкостью ее введения: легче всего снимается защита у альдегидов, затем идут кетоны и хуже всех - у ос, р-непре-дельных кетонов. Кетали стерически затрудненных кетонов приходится долго кипятить в минеральной кислоте. Их иногда удается снимать в нейтралъ-йых условиях при действии слабоосновных ацетоновых или спиртовых растворов или никеля Ренея. [9]
Конденсация [2, 23, 24] альдегидов и кетонов с гидроксил-амином ( образующимся in situ из соли при действии основания) и О-замещенными гидроксиламинами, приводящая к оксимам и О-замещенным оксимам, обычно протекает легче, чем конденсация аминов с карбонильными соединениями. Оксимирование подобно образованию шиффовых оснований катализируется кислотами, но его обычно проводят в буферном растворе ( например, в фосфатном буферном растворе) при рН - 4, чтобы обеспечить оптимальную скорость реакции. Оксимирование стерически затрудненных кетонов рекомендуют проводить в основной среде. Вместо гидроксиламина для оксимирования альдегидов и кетонов можно использовать динатриевую соль гидроксиламиндисуль-фоновой кислоты HON ( SO Na) 2, которую можно легко приготовить in situ пропусканием диоксида серы в водный раствор нитрита натрия и бисульфита натрия. [10]
Реактивы Гриньяра ведут себя как сильные нуклеофилы, и реакция их присоединения практически необратима. Однако важно подчеркнуть, что реакции с реактивами Гриньяра, в частности реакции присоединения к группе СО, представляют собой общий метод связывания различных групп с атомом углерода, поскольку спирты, первоначально получаемые как продукты реакции, далее могут быть модифицированы с помощью самых разнообразных реакций. В прошлом аналогично использовали цинкорганические соединения, которые затем все более вытеснялись реактивами Гриньяра; реактивы Гриньяра в свою очередь сейчас все больше вытесняются литий-алкилами RLi и литийарилами ArLi. Эти реактивы дают больше продуктов присоединения нормального строения при взаимодействии со стерически затрудненными кетонами, а также больше продуктов 1 2 - и меньше продуктов 1 4-присоединения при взаимодействии с системой СС-С О, чем реактивы Гриньяра ( ср. [11]
Реакции проводят путем прибавления раствора 0 03 моля кетона в 10 мл эфира и 0 055 моля металлоорганического соединения ( RLi, RMgX) в 15 мл эфира под азотом и при нагревании в течение 4 час. По окончании реакции прибавляют 4 мл циклогек-сана, реакционную смесь обрабатывают обычным образом и разгоняют на колонке. Полученные фракции подвергают хроматографическому анализу. Полученные результаты показывают, что с усложнением пространственного строения кетона ( увеличение стери-ческих препятствий) изменяется и относительная реакционная способность ос-атомов водорода в отношении отрыва гидрид-иона. Условия синтеза карбинолов из стерически затрудненных кетонов с участием RLi ( при низкой температуре) приведены ниже. [12]
Страницы: 1