Килограмм-молекула
Cтраница 3
При ректификации числом флегмы называется отношение числа килограмм-молекул флегмы к числу килограмм-молекул дистиллята или количество килограмм-молекул флегмы, приходящееся на 1 кмоль дистиллята. [31]
В расчете приняты следующие обозначения: ПА и п-в - соответственно количество килограмм-молекул азота и кислорода в исходной смеси и X-количество килограмм-молекул моноксида азота в равновесной смеси. [32]
Итак, количество килограммов газа, равное его молекулярному весу, называется килограмм-молекулой, или молем. [33]
При горении газообразных веществ определение количества воздуха несколько упрощается, так как объем килограмм-молекулы различных газов при одной и той же температуре и давлении одинаков. Приняв условно объем молекулы газов равным 1 м3, производят соответствующие вычисления. [34]
Килограмм-молекула ( Моль) - величина в 1000 раз большая грамм-молекулы; например, килограмм-молекула кислорода равна 32 кг, килограмм-молекула азота 28 016 кг. [35]
Весовое количество М кг газа ( где М - молекулярный вес) носит название килограмм-молекулы. Таким образом, уравнение Mv const свидетельствует, что объем одной килограмм-молекулы для данных температуры и давления для всех газов есть величина постоянная. [36]
Произведение удельного объема ( v) на молекулярный вес ( ц) выражает объем одной килограмм-молекулы или моля газа ( v i: zii) - Равенство ( 13) показывает, что объем одного моля ( v) - величина постоянная для всех идеальных газов при одинаковых Давлениях и температурах. [37]
Расчет процесса горения в объемных единицах основан на следствии из закона Авогадро, по которому килограмм-молекула любого вещества, находящегося в газообразном состоянии, занимает объем 22 4 мя. [38]
При ректификации числом флегмы называется отношение числа килограмм-молекул флегмы к числу килограмм-молекул дистиллята или количество килограмм-молекул флегмы, приходящееся на 1 кмоль дистиллята. [39]
Масса вещества, выраженная в килограммах и численно равная его молекулярному весу jx, называется килограмм-молекулой, или кил о молем. [40]
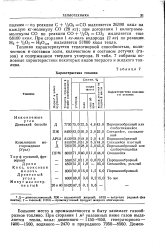 |
Характеристика топлива. [41] |
СО выделяется 26390 ккал на каждую кг-молекулу СО ( 28 кг); при догорании 1 килограмм-молекулы СО по реакции СО / 2О2 СО2 выделяется еще 68100 ккал. [42]
Если же указанную величину выразить в единицах веса, получим грамм-атом, грамм-молекулу, килограмм-атом, килограмм-молекулу. Грамм-атом - это количество граммов элемента, численно равное его атомному весу. Соответственно определяются грамм-молекула, килограмм-молекула, килограмм-атом. [43]
Численное значение универсальной газовой постоянной зависит от того, в каких единицах измерены нор - V0 одной килограмм-молекулы газа. [44]
Весовое количество ( д, ( кг) газа ( г - молекулярный вес) носит название килограмм-молекулы или кил о моля. Объем киломоля при одинаковых температурах и давлениях для всех газов одинаков. [45]
Страницы: 1 2 3 4