Кильпатрик
Cтраница 2
Kilpatrick, Illinois Institute of Technology): Работа, доложенная д-ром Мертеллом ( статья 33), должна приобрести большую убедительность, если учесть данные некоторых опытов, отсутствующих в названной работе. Кильпатрик и Кильпатрик [5] показали, что гидролиз ДФФ относится к общему случаю щелочного катализа и в соответствии с этим взглядом комплексы, не содержащие меди, также должны оказывать каталитическое действие. [16]
Kilpatrick, Illinois Institute of Technology): Работа, доложенная д-ром Мертеллом ( статья 33), должна приобрести большую убедительность, если учесть данные некоторых опытов, отсутствующих в названной работе. Кильпатрик и Кильпатрик [5] показали, что гидролиз ДФФ относится к общему случаю щелочного катализа и в соответствии с этим взглядом комплексы, не содержащие меди, также должны оказывать каталитическое действие. [17]
Равновесие этой реакции изучалось рядом исследователей - первоначально Будуар, позднее Майер, Фальк и другие. Наиболее поздние исследования равновесия окиси углерода и углекислоты над графитом были проведены Кильпатриком и другими. [18]
В табл. 15 приведены теплоты сгорания и образования из элементов паров алкинов. Величины для первых семи углеводородов найдены Прозеном и Россини и опубликованы в статье Вегмена, Кильпатрика, Питцера и Россини [14] без указания каких-либо сведений о чистоте препаратов и методике определения. [19]
В зависимости от температуры и давления конверсии в реакци-шном газе содержится большее или меньшее количество метана i продуктов его реакции с водяным паром и кислородом. Равноосный состав газа конверсии при различных температурах и нор-лальном давлении рассчитан А. А. Введенским [24] по данным ра-от Вагмана, Кильпатрика, Тейлора, Питцера и Россини. [20]
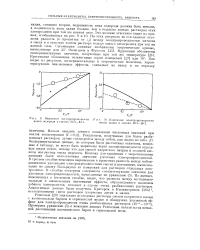 |
Изменение электропроводности [ IMAGE ] Изменение электропроводности иоиои водорода в смесях H ( U-K ( U. ноиои калия в смесях НС1 - КС1. [21] |
Экспериментальные данные, по которым был к рассчитаны величины, вошедшие в таблицу, не могут быть выражены через электропроводности отдельных видов ионов, потому что для смесей хлористого натрия и соляной кислоты неизвестны числа переноса. Поэтому для сравнения с теоретическими данными были использованы значения удельных электронроводностей. Из данных, помещенных в последнем столбце, видно, что разность между экспериментальным и вычисленным значениями эффекта, обусловленного наличием добавок электролитов, исчезает в случае очень разбавленных растворов. Аналогичные данные были получены Кригером и Кильпатриком [ 28a ] J, исследовавшими смеси растворов хлористых лития и калия. [22]
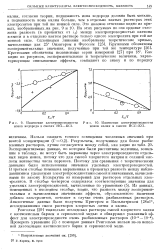 |
Изменение электропроводности [ IMAGE ] Изменение электропроводности ионов водорода в смесях НС1 - КС1. ионов калия в смесях НС1 - КС1. [23] |
Экспериментальные данные, по которым были рассчитаны величины, вошедшие в таблицу, не могут быть выражены через электропроводности отдельных видов ионов, потому что для смесей хлористого натрия и соляной кислоты неизвестны числа переноса. Поэтому для сравнения с теоретическими данными были использованы значения удельных электропроводностей. В третьем столбце помещена выраженная в процентах разность между наблюдавшимися удельными электрон роводностями смесей и значениями, вычисленными по закону Кольрауша из измерений для растворов отдельных электролитов. Из данных, помещенных в последнем столбце, видно, что разность между экспериментальным и вычисленным значениями эффекта, обусловленного наличием добавок электролитов, исчезает в случае очень разбавленных растворов. Аналогичные данные были получены Кригером и Кильпатриком [ 28а ] 1, исследовавшими смеси растворов хлористых лития и калия. [24]
Циклопентан, алкилциклопентаны и диметилциклопен-таны. Там же приводятся термодинамические величины алкилциклопентанов, вычисленные Кильпатриком, Вернером, Беке-том, Питцером и Россини [14] приближенными методами. [25]
По их мнению, эти колебании обусловлены загрязнениями исходных растворов. Они нашли, что при применении воды и нестабилияированной перекиси водорода, не содержащих ныли, квантовый выход равен лишь небольшой-доле ранее полученных значений. Так, раствор НгОг, свободный от пыли, выделяет лишь 1 мл кислорода, тогда как загрязненный раствор за то же время выделяет 300 мл. На основании своих опытон Раис и Кильпатрик пришли к выводу, что разложение НиОг ш; отклоняется от фотохимического закона. Зависимость квантошп) ныхола от чистоты растворен заставляет полагать, что фотохимическое разложение перекиси водорода является цепной реакцией, причем стенки сосуда и пылинки дают толчсж для начали цепи. [26]
Страницы: 1 2