Кинетика - инактивация
Cтраница 1
Кинетика инактивации описывается экспонентой, при этом характеристическое время инактивации определяется константой скорости инактивации этого лабильного фермента. [1]
Изучена кинетика инактивации и мутагенная эффективность в индукции мутаций типа замены пар оснований у S. [2]
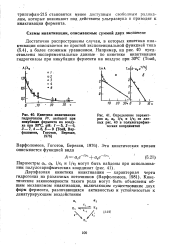
Изучение кинетики инактивации различных биологических структур под действием химических мутагенов представляет собой и теоретический и практический интерес. Характер кривой инактивации позволяет сделать выводы о первичных механизмах взаимодействия биологического материала с мутагенным агентом и судить об участии в этом процессе ферментных систем репарации. В практических целях на основе исследования биологически допустимых доз каждого из используемых химических мутагенов представляется возможность - выбрать оптимальные дозы для каждой конкретной задачи исследования. [3]
Соответственно из анализа кинетики инактивации можно получить информацию о величине этих параметров и решить вопрос о том, какая стадия является лимитирующей и какой фермент цепи является наиболее неустойчивым с точки зрения инактиви-рующего воздействия. [4]
Достаточно распространены случаи, в которых кинетика инактивации описывается не простой экспоненциальной функцией типа (5.4), а более сложным уравнением. [6]
Если обратимые конформационные изменения протекают относительно быстро и в каждый момент времени конформационные равновесия успевают устанавливаться, кинетика инактивации будет описываться одноэкспоненциальным уравнением, однако G наблюдаемую константу скорости инактивации будут входить константы равновесия конформационных изменений. [7]
Систематических исследований перемещения вирусов в реках практически нет, а многочисленные наблюдения наличия или отсутствия, вирусных частиц не учитывают должным образом кинетику инактивации вирусов. Не было обнаружено ни значительных потерь вирусных частиц, ни изменения их литических свойств. Выживаемость фага в реке была также высока, как и в ранее проведенных экспериментах. [8]
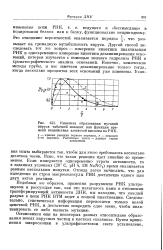 |
Кинетика образования мутаций вируса табачной мозаики как функция времени воздействия азотистой кислоты на РНК. [9] |
Это отношение вероятностей оказывается порядка у, что указывает на громадную мутабильность вируса. Другой способ исследовать тот же вопрос - измерение кинетики инактивации РНК и одновременное измерение кинетики дезаминирования оснований, которая изучается с помощью полного гидролиза РНК и хроматографического анализа оснований. Конечно, химические методы грубы, и мы замечаем дезаминирование только тогда. [10]
Вид зависимости характеризуется двумя параметрами - средним временем и дисперсией среднего времени. Кинетика инактивации в этом случае характеризуется периодом индукции, который сменяется быстрой потерей активности. [12]
Интересные экспериментальные результаты получены при изучении конформационных изменений белка, сопряженных с изменением рН и перераспределением зарядов на белковой глобуле. Как правило, инактивация ферментов существенно возрастает или замедляется в сильнокислых или щелочных растворах. В работе Клибанова, Мартинека, Березина ( 1974) проведено изучение кинетики инактивации химотрипсина под действием ультразвука. [13]
Таким образом, обсуждаемая выше инактивация гидрогеназы в присутствии кислорода протекает с участием по крайней мере двух состояний фермента. В механизме катализа гидрогеназами кинетический процесс, характеризуемый временем Т2, в отсутствие кислорода практически не имеет места. В этих условиях кинетика процесса, характеризуемая параметром ть отражает, по-видимому, тепловую денатурацию белка. В присутствии кислорода появляется второй экспоненциальный член в кинетике инактивации. В этих условиях происходят, по-видимому, процессы окисления функционально важных групп активного центра фермента, что влечет за собой его необратимую инактивацию. [14]
Страницы: 1