Кинетика - коррозия
Cтраница 4
Рассмотренный случай является типичным и простейшим для общего представления о кинетике коррозии, тем не менее показанные зависимости позволяют оценить возможные изменения механизма и скорости электродных реакций. Прежде всего из них следует обобщающий вывод о том, что любые внутренние и внешние факторы, определяющие механизм и скорость электродных реакций, в конечном счете сказываются на характере изменения поляризационных кривых. В этой связи ниже кратко обсуждаются наиболее существенные закономерности, определяющие кинетику коррозионных процессов, которые могут быть полезными при оценке возможности электрохимических способов защиты от коррозии. [46]
 |
Кипетика коррозии и образования защитной пленки на поверхности винца. [47] |
Одновременное исследование кинетики образования защитных пленок на поверхности свинцовых пластинок и кинетики коррозии их показало, что все индивидуальные серу-и фосфорсодержащие соединения, так же как и упомянутые выше товарные антикоррозионные присадки, образуют на поверхности свинца защитную пленку, которая тормозит коррозию металла. [48]
Из совместного рассмотрения кинетики образования защитных пленок серой и фосфором и кинетики коррозии свинца следует, что до шести часов работы свинцовой пластинки в масле на аппарате Пинкевича при температуре 140 на поверхности свинца образуется защитная пленка, содержащая как серу, так и фосфор, и эффективно тормозящая развитие коррозии. [49]
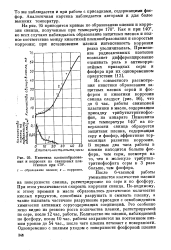 |
Кинетика пленкообразования и коррозии на свинцовых пластинках при 170. [50] |
Из совместного рассмотрения кинетики образования защитных пленок серой и фосфором и кинетики коррозии свинца следует ( рис. 96), что до 6 час. Пинкевича при температуре 140 на поверхности свинца образуется защитная пленка, содержащая серу и фосфор, эффективно тормозящая развитие коррозии. [51]
Эта или другая аналогичная экспериментальная зависимости могут быть использованы при исследовании кинетики коррозии на аналоговых моделях. [52]
Следует отметить, что отдельные попытки получить более достоверные данные о кинетике коррозии металлов ( с помощью этой методики) имели место, но они преследовали иные конечные цели. [53]
Однако термодинамическая неустойчивость металлов, характеризуемая электродным потенциалом, не определяет однозначно кинетики коррозии. Скорость протекания анодной и катодной ре - О акций и, следовательно, скорость коррозии согласно законам элек - трохимической кинетики определяется общим значением потенци - ала на границе металл - раствор, составом раствора и условиями ии компонентов или продуктов реакции в растворе, явле-поляризации. [54]
 |
Схема ступенчатого изменения температуры металла. [55] |
Ниже приводятся основы расчета характеристик высокотемпературной коррозии металла исходя из основной формулы кинетики коррозии и заданной закономерности изменения температуры со временем. Рассматриваются характеристики коррозии при ступенчатом и непрерывном изменении температуры. [56]
Особое внимание уделено долгосрочному прогнозированию по данным расчетов, основанных на определении кинетики коррозии бетонов в указанных агрессивных средах. Излагается методика расчета долговечности бетона, основанная на том, что потеря несущей способности бетона пропорциональна весовым потерям, обусловленным коррозией цементного камня. [57]
Наблюдения за ингибитирующим влиянием добавок, введенных в углеводородную фазу среды, на кинетику коррозии той части металлической поверхности, которая находится в водной фазе среды, свидетельствуют о постепенном снижении во вре - мени общей скорости растворения металла. Сначала поверхность образцов интенсивно корродирует в объеме водной фазы, на что указывает бурное выделение пузырьков водорода. Затем скорость процесса выделения водорода начинает снижаться, что не связано с изменением рН среды. [58]
В связи с этим большое значение приобретает тщательный анализ имеющегося массива информации по кинетике коррозии цементного камня, выявление ее закономерностей и механизма. [59]
Таким образом, учитывая изложенное, можно считать установленным наличием единой ( общей) кинетики коррозии различных металлов в других активных средах. [60]
Страницы: 1 2 3 4 5