Кинетика - процесс - кристаллизация
Cтраница 1
Кинетика процесса кристаллизации сильно зависит от формы растущих кристаллов. В настоящей работе рассмотрена кристаллизация кристаллов игольчатой формы, которая является следствием одномерного роста кристаллов при встраивании молекулы кристаллизующегося вещества только в одну грань растущего кристалла. [1]
Кинетика процесса кристаллизации и фазового превращения полугидрата сульфата кальция определяется температурным режимом, скоростью смешения реагентов и их концентрацией. Скорость образования зародышей кристаллов сульфата кальция зависит от концентрации используемой серной кислоты и температуры. В то же время снижение концентрации H2SO4 хоть и приводит к образованию более крупных кристаллов полугидрата, может быть использовано с известными ограничениями. Они связаны со скоростью разложения фосфатного сырья. Увеличение температуры в общем оказывает положительное влияние как на кристаллизацию полугидрата, так и на скорость разложения. Однако повышение Т может быть произведено в разумных пределах в зависимости от оптимального варианта технологии получения суперфосфата как такового. [2]
Кинетика процесса кристаллизации синдиотактического полипропилена изучена в меньшей степени. Одно из таких исследований принадлежит Родриге-су - Арнольду с соавт. Значение температуры плавления кристаллической фазы составляло около 160 С, что существенно превышает аналогичную характеристику коммерческого синдиотактического полипропилена; более высокой оказалась и скорость кристаллизации. Чоя и Уайта [64], изучавших низкотактический Синдиотактический полипропилен, было показано, что скорость кристаллизации у этого полимера существенно ниже, чем у высоко-изотактичного полипропилена Циглера-Натты. [3]
Кинетика процесса кристаллизации синдиотактического полипропилена изучена в меньшей степени. Одно из таких исследований принадлежит Родриге-су - Арнольду с соавт. Значение температуры плавления кристаллической фазы составляло около 160 С, что существенно превышает аналогичную характеристику коммерческого синдиотактического полипропилена; более высокой оказалась и скорость кристаллизации. Чоя и Уайта [64], изучавших низкотактический синдиотактический полипропилен, было показано, что скорость кристаллизации у этого полимера существенно ниже, чем у высоко-изотактичного полипропилена Циглера-Натты. [4]
Кинетику процесса кристаллизации предложено описывать или уравнением I порядка с возрастающей энергией активации [6, 7] или при помощи. При этом в обоих случаях получается широкий набор энергий активации. [5]
На кинетику процесса кристаллизации влияет большое число факторов, из которых основными являются: пересыщение, температура, интенсивность перемешивания. Количественный эффект воздействия того или иного фактора определяется экспериментально для конкретной системы. [6]
Статика и кинетика процесса кристаллизации должны быть особенно тщательно учтены при проектировании кристаллизационной аппаратуры, которое в основном можно разбить на два этапа: балансовый расчет и кинетический. [7]
Согласно теории кинетики процесса кристаллизации, предложенной Аврами, существует определенная вероятность образования активного центра кристаллизации в единицу времени. Зависимость этой вероятности от температуры определяется двумя факторами. Первый из них соответствует диффузии и аналогичен числу столкновений в газе, другой определяется энергией активации, необходимой для образования центра. [8]
Влияние МП на кинетику процесса кристаллизации пред-тавляет немалый практический интерес в связи с возражающим использованием магнитных воздействий в техно-югических процессах, сопровождаемых кристаллизацией i образованием кристаллизационных структур. [9]
В работах [103-105] была исследована кинетика процесса кристаллизации на основании вышеизложенной модели при условии, что п1 и mmax - - максимальный размер кристалла. Эти предположения могут быть приняты в качестве первого приближения, но их уточнение было бы весьма желательно. Действительно, всегда существует некоторая вероятность того, что настоящий кристалл-лидер не окажется в пробе, отобранной для дисперсионного анализа; возможна ошибка и в противоположную сторону, когда в качестве кристалла-лидера будет зафиксирован кристалл, выросший на случайной затравочной частице, находившейся в растворе или на стенке сосуда до начала кристаллизации. Уточнение величин / птат и п требует дополнительной информации. [10]
Упрощенное выражение (4.3) является уравнением кинетики процесса кристаллизации. [11]
Следуя Аврами, Морган ш оценил кинетику процесса кристаллизации для основных возможных видов зародышеобразования и процессов роста кристаллической фазы. [12]
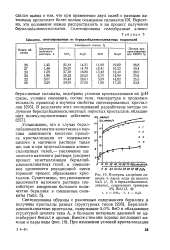 |
Цеолиты, синтезированные из бериллийалюмосиликатных гидрогелей.| Изотермы адсорбции аммиака и паров воды на цеолите NaA ( 1, 2 и бериллийалюмоси-ликатах, содержащих примерно 5 % ВеО ( 3, 4. [13] |
Установлено, что в случае бериллийалюмосиликатов качественная картина зависимости кинетики процесса кристаллизации от содержания щелочи в маточном растворе такая же, как и при кристаллизации алюмо-силикатных гелей - увеличение ще лочности маточного раствора ускоряет процесс кристаллизации бериллийалюмосиликатных гелей, а уменьшение щелочности реакционной смеси тормозит процесс образования кристаллов. [14]
Мэль и Бокрис619 получили значение гс при предположении о кинетике процесса кристаллизации, экспериментально еще не подтвержденной. [15]
Страницы: 1 2 3 4