Кинетика - каталитический процесс
Cтраница 1
Кинетика каталитических процессов рассмотрена во многих книгах [2, 5, 7, 9, 12, 14, 20-21, 23-26], поэтому в данной монографии только напомним некоторые представления для рассмотрения процессов катализа в кипящем слое. [1]
Для кинетики каталитических процессов на неоднородных поверхностях важное значение приобретает возможное изменение энергии активации каталитической реакции с изменением степени заполнения поверхности. При хемосорбционном механизме гетерогенного катализа изменения Qanc и Еаяо со степенью заполнения поверхности должны неизбежно приводить к зависимости энергии активации каталитического процесса от заполнения. Кат с изменением заполненности и состава адсорбционной фазы представляют ведущий фактор каталитической кинетики на неоднородных поверхностях. [2]
Исследование кинетики каталитических процессов начинают с изучения свойств и поведения катализатора в различных условиях. Вследствие сказанного работы по технологии и автоматизации процессов иногда значительно опережают работы по изучению кинетики. [3]
Исследование кинетики каталитических процессов - одним из основных методов определения механизма катализа, знание которого необходимо для решения проблем научного и практического плана Кинетические данные при этом должны быть надежными и неискаженными макроскопическими факторами. [4]
Исследование кинетики каталитических процессов начинают с изучения свойств и поведения катализатора в различных условиях. Вследствие сказанного работы по технологии и автоматизации процессов иногда значительно опережают работы по изучению кинетики. [5]
При исследовании кинетики каталитических процессов и активности катализаторов необходимо определение концентраций исходных веществ и продуктов реакции. [6]
Данные по кинетике газофазного каталитического процесса дегидрохлорирования пентахлорэтана и несимметричных хлорэтанов практически отсутствуют. Приведенный выше ряд свидетельствует, что они дегидрохлорируются, как правило, с большей скоростью, чем симметричные хлорэтаны. Можно отметить, что скорость дегидрохлорирования 1 1 - С2Н4С12 на оксиде алюминия при 340 С примерно в 1 5 раза выше, чем для 1 2 - С2Н4С12, а хлорид бария активирует процесс разложения пентахлорэтана на угле при 200 - 350 С. [7]
Вопросы изучения катализаторов и кинетики каталитических процессов взаимно связаны между собой. [8]
Для получения информации о кинетике каталитического процесса необходимы знания состава газа и температуры на каталитической поверхности. Во многих случаях применение адиабатического интегрального реактора или импульсного микрореактора дает возможность обойтись без таких исходных данных. Другие реакторы применимы до известной степени; для изотермического интегрального реактора - необходимо предварительное создание модели соответствующего процесса, а дифференциальные могут быть оценены непосредственно. Информация о кинетике процесса полезна не только в фундаментальных исследованиях механизма реакции и каталитической активности хорошо идентифицированных каталитических поверхностей, но также при проектировании реакторов и оптимиза-пии процесса. Знание кинетических характеристик может сильно упростить разработку модели процесса, а также уменьшить количество данных, необходимых для адекватного описания процесса. [9]
Проведенное рассмотрение позволяет предположить, что кинетика каталитических процессов в апротонных растворителях может быть более сложной, чем в водных растворах, несмотря на кажущуюся химическую простоту системы. Этот общий вывод следует из существующего экспериментального материала, который, правда, еще не совсем осмыслен. В частности, скорость реакции редко бывает прямо пропорциональной концентрации катализатора, а наблюдаемый порядок иногда больше, иногда меньше единицы. Такая особенность может соответствовать кинетическим предсказаниям, сделанным в предыдущем абзаце. Однако возникают дополнительные сложности, обусловленные тем, что катализаторами, обычно используемыми в этих исследованиях, явля ются кар-боновые кислоты, которые ассоциированы в апротонных растворителях в разной степени. [10]
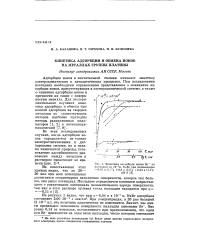 |
Кинетика адсорбции ионов Вг - на палладии из 10 - 3н. NaBr при потенциалах - 0 05 в ( 1 1, 0 2 в ( 2 2, 0 54 в ( 3 3. рН 3. [11] |
Адсорбция ионов в значительной степени изменяет кинетику электрохимических и каталитических процессов. При исследовании последних необходимы определенные представления о механизме адсорбции ионов, присутствующих в электрохимической системе, а также о кинетике адсорбции ионов и прочности их связи с поверхностью металла. [12]
С этих же позиций могут быть объяснены наблюдаемые закономерности кинетики каталитических процессов. [13]
Основным методом изучения механизма катализа остается все же изучение кинетики каталитических процессов. Изучение кинетики необходимо также для оценки каталитических свойств контактов и для выбора оптимального режима ведения процесса. [14]
Основным методом изучения механизма катализа остается все же изучение кинетики каталитических процессов. Изучение кинетики необходимо также для оценки каталитических свойств контактов и для выбора оптимального рекима ведения процесса. [15]
Страницы: 1 2 3 4