Кинетика - сложный процесс
Cтраница 1
Кинетика сложных процессов, включающих химические и физические стадии, является предметом рассмотрения в специальном разделе кинетики - макрокинетике. ПРИ описании кинетики гетерогенных реакций приходится включать элементы макрокинетики. [1]
При изучении кинетики сложных процессов первой задачей является установление лимитирующих стадий. [2]
Воздействие растворителя на кинетику сложного процесса в целом заключается, собственно говоря, во влиянии его на скорость элементарных реакций. Понятие об элементарной реакции в жидкой фазе лишено той определенности, которую оно имеет для газофазных реакций. Элементарная реакция как акт взаимодействия двух частиц в растворе не может происходить из-за присутствия большого числа молекул растворителя, принимающих непосредственное участие в реакции. [3]
Фундаментальные исследования по изучению кинетики сложного процесса распада ПВХ в присутствии металлсодержащих стабилизаторов только начинают развиваться. [4]
Из сказанного следует, что первая задача при изучении кинетики сложных процессов - установление лимитирующих стадий. [5]
Используя теорию случайных процессов, можно показать, что в стохастических системах левая часть уравнения (2.1) сводится к конечному числу функционалов, позволяющих описать кинетику сложных процессов в поликомпонентных системах в рамках феноменологического подхода. [6]
В настоящей главе подробно обсуждаются характерные свойства кинетических механизмов реакций, методы анализа механизмов реакций, основные принципы их упрощения и различные следствия математического моделирования кинетики сложных процессов. Эти аспекты представляют определенный интерес, поскольку в некоторых случаях необходимы механизмы реакций, включающие более 1000 различных химических компонентов, для описания процессов, протекающих в гомогенном реакторе ( см. гл. Такие огромные кинетические механизмы требуют и столь же грандиозных вычислительных затрат при моделировании процессов горения в двигателях и горелках из-за пространственно неоднородной структуры трехмерных турбулентных потоков с изменяющимися концентрациями и температурой, которые наблюдаются в них. [7]
Пг, tij - концентрации частиц сортов i, j, общее число которых w, Hi - скорости возникновения этих частиц независимо от их взаимного превращения; ац - коэффициенты, выражающие обобщенные константы скорости взаимного превращения частиц; 25 - - коэффициенты диффузии частиц; А - знак оператора Лапласа. Эта система в общем виде описывает кинетику сложных процессов превращения молекул и атомов, к числу которых могут быть отнесены как химические реакции, протекающие через сопряженные системы кинетических звеньев, как цепные реакции, протекающие через свободные радикалы, так и физические процессы возбуждения молекул и атомов, имеющие место в явлениях фотовозбуждения и в холодной плазме электрических разрядов, где роль свободных радикалов выполняют возбужденные атомы и молекулы, находящиеся на разных уровнях возбуждения. [8]
Эта система в общем виде описывает кинетику сложных процессов превращения молекул и атомов, к числу которых могут быть отнесены как химические реакции, протекающие через сопряженные системы кинетических звеньев, как цепные реакции, протекающие через свободные радикалы, так и физические процессы возбуждения молекул и атомов, имеющие место в явлениях фотовозбуждения и в холодной плазме электрических разрядов. [9]
В последнем разделе обсуждаются особенности других возможных стадий электродных процессов - химических и образования новой фазы, а также многостадийные и параллельные процессы и роль явлений пассивности и адсорбции органических соединений в электрохимической кинетике. В этом разделе отражены только самые основные особенности кинетики сложных процессов и приведено ограниченное число примеров практически важных электрохимических реакций. [10]
Наблюдаемые зависимости могут быть следствием как термодинамических, так и кинетических особенностей данного процесса. К сожалению, имеющиеся к настоящему времени данные по термодинамике и кинетике сложных процессов роста из пара легированных кристаллов недостаточны для однозначного объяснения полученных результатов. В этой ситуации представляется целесообразным сопоставить наблюдаемые зависимости с кинетикой роста слоев и выявить корреляционные связи. [12]
Сложный гетерогенно-каталитический аро-цесс включает ряд стадий адсорбции и десорбции исходных веществ, промежуточных и конечных продуктов и реакций взаимных превращений веществ, адсорбированных на активной поверхности. Полное число стадий может быть весьма велико, и, чтобы разобраться в кинетике сложного процесса, необходимо учесть обычно наблюдаемые резкие различия между скоростями отдельных стадий. [13]
Из схемы универсального последовательного анализа ( см. рис. 14) видно, что этап стехиометрического анализа предшествует кинетическому. Он, однако, не просто предшествует ему, но и лежит в основе последнего, поскольку балансовые ограничения носят принципиальный характер и, являясь одной из форм закона сохранения вещества, в значительной степени определяют основные особенности кинетики сложного процесса. Перечислим конкретные задачи начального этапа анализа. [14]
 |
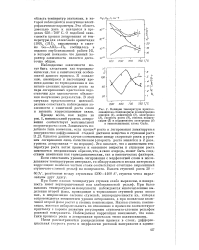
Дифрактограммы ZnS-Cl. [15] |
Страницы: 1 2