Кинетика - подобный процесс
Cтраница 1
Кинетика подобных процессов описывается в следующем параграфе. Легко указать примерный ход такого процесса. [1]
Для расчетов кинетики подобных процессов часто используется обобщенный принцип Флори, в котором учитывается взаимная зависимость только между активными центрами, расположенными в молекуле достаточно близко друг от друга, а влиянием остальных факторов на реакционную способность активных центров можно пренебречь. При таком подходе, как и в случае независимых активных центров, все результаты по расчету кинетики могут быть выражены в терминах сравнительно небольшого числа констант скоростей элементарных реакций. [2]
Большинство исследователей, рассматривая кинетику подобных процессов, предлагают схемы, основанные на сравнительно простых физических предпосылках и совпадающие друг с другом в основных пунктах. [3]
В настоящей главе обсуждаются результаты экспериментальных исследований кинетики подобных процессов в инертных растворителях и в газовой фазе. Эти результаты получены главным образом методами ЯМР и кинетической ИК-спектроскопии. Что касается теоретических аспектов рассматриваемой проблемы, то они еще не получили должного развития. Несколько работ, относящихся к этим проблемам, посвящено рассмотрению простейших модельных процессов. Особое внимание здесь будет обращено на влияние электронного строения взаимодействующих молекул на скорость процесса и на сравнение статических и динамических свойств водородной связи. [4]
На рисунке для сравнения представлены точки, полученные обычным методом эксперимента, когда факторы варьировались поочередно. Их хорошее совпадение свидетельствует о перспективности применения методов математического планирования к исследованию кинетики подобных процессов. [5]
Некоторые реакции сшивания, например отверждение продуктов взаимодействия диодов и эпоксидов, уже были описаны в разд. В этом разделе будет рассмотрено отверждение ненасыщенных сложных полиэфиров, сшивание 1 4-полидие-нов - 1 3, полполефинов и полисилоксанов. Изучение кинетики подобных процессов часто весьма затруднено из-за нерастворимости конечного трехмерного продукта. Во многих случаях такие процессы идут с понижением скорости во времени и не с очень высоким выходом. [6]
В отличие от реакций, подобных (2.2), продукты которых состоят только из одного цикла, образующихся в процессах трехмерной поликонденсации, макромолекулы могут содержать любое число подобных циклов произвольной длины. Аналогичная ситуация возможна в процессах трехмерной полимеризации и сшивания полимеров. Расчет кинетики подобных процессов с учетом реакции циклизации является весьма сложной-задачей, в настоящее время еще не решенной до конца. [7]
Подстановка опытных данных дает для толщины диффузионного слоя s величину около 10 - 8 см и меньше. Присутствие посторонних адсорбированных веществ на поверхности твердого тела может сильно влиять на скорость. При гетерогенных процессах, сопровождающихся образованием новой фазы ( как напр, кристаллизация из пересыщенных растворов), фактором, определяющим течение процесса, является уже не диффузия: кинетика подобных процессов зависит от скорости образования зародышей и от быстроты их роста. Чем в большей степени переохлажден пересыщенный раствор, тем ббльшую величину приобретает скорость образования зародышей, которая в определенной точке достигает своего максимума и при дальнейшем понижении t начинает замедляться. Скорость роста кристаллов измеряется приращением их линейных размеров в единицу времени. [8]
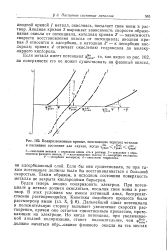 |
Поляризационные кривые, поясняющие переход металла в пассивное состояние для случая, когда ср аевн f s cf H. [9] |
Будем теперь анодно поляризовать электрод. При потенциале ф металл должен окисляться, посылая свои ионы в раствор. В этих условиях мы имеем активный анод, беспрепятственно растворяющийся. Кинетика подобного процесса была рассмотрена выше ( гл. Дальнейший сдвиг потенциала в положительную сторону вызывает увеличение скорости растворения, причем оно остается единственным процессом, протекающим на электроде. [10]
Будем теперь анодно поляризовать электрод. При потенциале р металл должен окисляться, посылая свои ионы в раствор. В этих условиях мы имеем активный анод, беспрепятственно растворяющийся. Кинетика подобного процесса была рассмотрена выше ( гл. Дальнейший сдвиг потенциала в положительную сторону вызывает увеличение скорости растворения, причем оно остается единственным процессом, протекающим на электроде. Но когда потенциал, при увеличиваемой анодной поляризации, станет положительнее, чем фр, должно начаться образование фазового окисла на тех местах поверхности, где это возможно. Этот процесс не в состоянии длительно протекать и ускоряться с ростом потенциала ( как это имело место для процесса Ме-Ме), ибо на тех участках, на которых образовался окисел толщиной в несколько элементов кристаллической решетки, дальнейшее образование его должно прекратиться. В этих местах поверхность металла больше не соприкасается с раствором. [11]
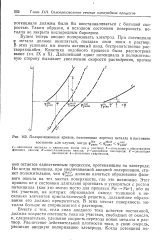 |
Поляризационные кривые, поясняющие переход металла в пассивное состояние для случая, когда ф аевн р аев ф н. [12] |
Будем теперь анодно поляризовать электрод. При потенциале Ф металл должен окисляться, посылая свои ионы в раствор. В этих условиях мы имеем активный анод, беспрепятственно растворяющийся. Кинетика подобного процесса была рассмотрена выше ( гл. [13]
Страницы: 1