Кинетика - химический процесс
Cтраница 1
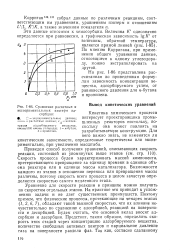 |
Сравнение расчетных и экспериментальных изотерм адсорбции. [1] |
Кинетика химического процесса интересует проектировщика промышленных реакторов постольку, поскольку она может повлиять на разрабатываемую конструкцию. [2]
Изучение кинетики химических процессов, используемых в промышленности, очень важно для инженера-технолога, так как позволяет установить оптимальные рабочие условия ( с технологической и экономической точек зрения, а также с точки зрения техники безопасности) и помогает при проектировании и расчете реакторов. [3]
Изучение кинетики химического процесса представляет собой сравнительно сложную задачу и требует выполнения исследовательских работ в значительном объеме. При этом следует иметь в виду, что изменение условий протекания процесса ( температуры, давления, концентрации и пр. В частности, процесс, протекающий в одних условиях в кинетической области, может при изменении этих условий перейти в диффузионную область и наоборот. Наиболее сложны закономерности протекания каталитических и цепных процессов, а также процессов, проходящих при одновременном получении нескольких целевых продуктов. [4]
Изучение кинетики химических процессов позволило сделать важные для практики управления химико-технологическими процессами выводы о том, что для повышения скорости реакции необходимо увеличивать начальные концентрации реагирующих веществ ( или давлений для реакций в газовой фазе), повышать температуру реакции, применять катализатор, увеличивать поверхность контакта взаимодействующих фаз в гетерогенных процессах. [5]
Изучение кинетики химического процесса представляет собой сравнительно сложную задачу и требует выполнения исследовательских работ в значительном объеме. При этом следует иметь в виду, что изменение условий протекания процесса ( температуры, давления, концентрации и пр. [6]
Моделирование кинетики химических процессов / Журн. [7]
Изучение кинетики химических процессов позволило сделать важные для практики управления химико-технологическими процессами выводы о том, что для повышения скорости реакции необходимо увеличивать начальные концентрации реагирующих веществ ( или давлений для реакций в газовой фазе), повышать тем-тературу реакции, применять катализатор, увеличивать поверхность контакта взаимодействующих фаз в гетерогенных процес -: ах. [8]
 |
Изменение числа молей п. ц реаги-рующего вещества вдоль реактора длины /. [9] |
Общие уравнения кинетики химических процессов в потоке можно получить, как это было показано Г. М. Панченковым, пользуясь методами гидродинамики. Этот прием интересен и важен в том отношении, что позволяет рассчитывать динамику как стационарных, так и нестационарных процессов. Полученные общие уравнения позволяют рассчитывать скорости как гомогенных реакций любых порядков и любой сложности ( необратимых, обратимых, параллельных, последовательных, автокаталитических, цепных и др.), так и гетерогенных ( см. гл. [10]
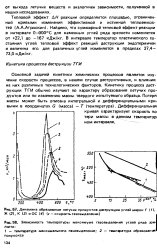 |
Динамика образования летучих продуктов деструкции углей марок Г ( Я, Ж ( 2, К ( 3 и ОС ( 4 ( v -скорость газовыделения.| Зависимость температуры максимума газовыделения углей ряда зр. [11] |
Основной задачей кинетики химических процессов является изучение скорости процессов, в нашем случае деструктивных, и влияния на них различных технологических факторов. Кинетику процесса деструкции ТГИ обычно изучают по характеру образования летучих продуктов или по изменению массы твердого испытуемого образца. [12]
Общие уравнения кинетики химических процессов в потоке можно получить, как это было показано Г. М. Панченковым, пользуясь методами гидродинамики. [13]
 |
Изменение числа молей ЯА. [14] |
Общие уравнения кинетики химических процессов в потоке можно получить, как это было показано Г. М. Панчен-ковым, пользуясь методами гидродинамики. Этот прием интересен и важен в том отношении, что позволяет рассчитывать динамику как стационарных, так и нестационарных процессов. Полученные общие уравнения позволяют рассчитывать скорости как гомогенных реакций любых порядков и любой сложности ( необратимых, обратимых, параллельных, последовательных, автокаталитических, цепных и др.), так и гетерогенных ( см. гл. [15]
Страницы: 1 2 3 4