Кинетика - распад - гидроперекись
Cтраница 1
Кинетика распада гидроперекисей в растворах имеет сложный характер, зависящий от условий протекания процесса. С изменением начальной концентрации гидроперекиси изменяется порядок реакции распада. [1]
Изучена кинетика распада гидроперекиси кумола, катализированного серной кислотой, в широком диапазоне смесей фенола и ацетона. [2]
 |
Кинетика распада гидроперекиси кумола в среде ацетофенона на смешанном кобальт-марганцевом катализаторе. [3] |
Исследована кинетика распада гидроперекиси кумола в среде ацетофенона с катализаторами - стеаратами кобальта, марганца и их смесью. Показано, что в ацетофеноне катализаторы дезактивируются в ходе реакции. [4]
Изучение кинетики распада гидроперекиси цпклогекспла и образования циклогексанона позволило установить, что циклогексанон образуется главным образом в результате непосредственного распада гидро-перекисного радикала. [5]
 |
Термостарение полиизопренового каучука в присутствии полисопряженных полимеров. [6] |
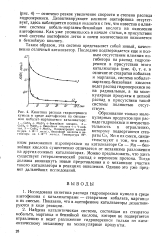
На рис. 19, 20 показана кинетика распада гидроперекиси изопропилбензола в присутствии различных антиоксидантов. [7]
Рассмотрим влияние концентрации катализатора, температуры и состава среды на кинетику нестационарной стадии и соответственно на кинетику распада гидроперекиси. Как видно из рис. 78, а и 83, а, стационарная интенсивность свечения, а следовательно, и стационарная скорость окисления достигаются тем быстрее, чем больше концентрация катализатора. [8]
В работах по разложению других гидроперекисей6 указывается, что характер расщада меняется в зависимости от состава среды, концентрации гидроперекиси и концентрации катализатора. Кинетика распада гидроперекиси носит сложный характер, зависящий от условий осуществления процесса. [9]
Строение гидроперекисей IV, V и VII доказано восстановлением их до соответствующих ацетиленовых спиртов, дигидроперекисей VI и VIII гидрированием до предельных гликолей анализом и ИК-спектрами. Показано, что кислород атакует Са - Н - связи в исходных углеводородах и в первую очередь третичные. Исследована кинетика распада гидроперекисей. [10]
Однако при этом надо иметь в виду, что скорость разветвления цепей отнюдь не равна непосредственно измеряемой скорости распада гидроперекисей. Дело в том, что кинетика распада гидроперекиси имеет сложный характер, зависящий от условий протекания процесса. [11]
Важной особенностью реакций, описываемых приведенной выше схемой, является то, что полная скорость реакции пропорциональна квадратному корню из скорости инициирования. Если же используется гидроперекись, то ее концентрация входит в выражение для скорости реакции в первой степени. Независимым путем было доказано, что в широком интервале условий кинетика распада гидроперекисей соответствует бимолекулярной реакции. [12]
Страницы: 1