Кинетика - анодное растворение - металл
Cтраница 1
Кинетика анодного растворения металлов должна зависеть не только от концентрации гидроксильных ионов, но и вообще от анионного состава р-аствора. Обычно принималось, что другие анионы в той или иной степени способны вытеснять ионы ОН - с поверхности растворяющегося металла и тем самым снижать их каталитическое действие. [1]
С практической точки зрения знание кинетики анодного растворения металла необходимо для правильного выбора токовых параметров процесса очистки. Кинетика анодного растворения металла определяется многими факторами, главными из которых являются скорость растворения, наличие в воде пластифицирующих веществ, замедляющих процесс растворения, и скорость отвода от поверхности электрода образующих продуктов растворения. [2]
Одним из серьезных затруднений при изучении кинетики анодного растворения металлов является изменение рельефа поверхности электрода во время опыта, устранить которое очень трудно. Поэтому многие исследования были проведены на жидких растворах изучаемых металлов в ртути. Если растворенные металлы менее благородны, чем ртуть, то атомы последней не участвуют в анодной реакции. Если скорость электродного процесса значительно меньше, чем скорость диффузии растворенного металла в ртути, то активность его в яоверхностном слое амальгамы остается постоянной, не внося искажении в изучаемый процесс. Вместе с тем, нет бесспорных оснований утверждать, что кинетика перехода атома металла через фазовый раздел должна быть тождественна в случае анодного растворения, протекающего на поверхности твердого металла, атомы которого образуют кристаллическую решетку, и этого же металла, растворенного в ртути. [3]
 |
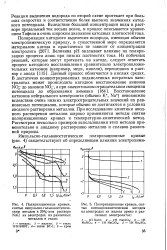
Анодная потенцио-статическая кривая для пассивируемого металла в присутствии анионов галогенов ( С1 -, В г или I. [4] |
Анионы С1 -, Вг, 1 - мало влияют на кинетику анодного растворения металлов в активной области или же несколько тормозят реакцию, как было показано выше. Но в пассивной области эти анионы часто вызывают депассивацию, причем электрод разъедается неравномерно, образуя питтинг. Такой вид коррозии очень опасен, так как, несмотря на малую потерю металла, на поверхности образуются глубокие язвы, препятствующие эксплуатации изделия. [5]
С практической точки зрения знание кинетики анодного растворения металла необходимо для правильного выбора токовых параметров процесса очистки. Кинетика анодного растворения металла определяется многими факторами, главными из которых являются скорость растворения, наличие в воде пластифицирующих веществ, замедляющих процесс растворения, и скорость отвода от поверхности электрода образующих продуктов растворения. [6]
Внесение поправки на эту реакцию путем алгебраического суммирования внешнего анодного тока и скорости выделения водорода ( найденной газометрически и выраженной в единицах плотности тока) приводит к получению линейного отрезка поляризационной кривой ( 4 на рис. 4.9), проходящего через точки анодной поляризационной кривой, лежащие при достаточно положительных потенциалах. Приведенные данные показывают, что кинетика анодного растворения металла остается одной и той же как в присутствии, так и в отсутствие параллельно протекающего процесса выделения водорода. [7]
Величина рН оказывает влияние на поляризацию процесса лишь при низких плотностях тока. Данный процесс облегчается в кислых средах. Восстановление катионов нейтрального электролита ( обычно К, Na) невозможно вследствие очень низких электроотрицательных значений их равновесных потенциалов, которые обычно не достигаются в условиях анодного растворения металлов. При исследовании кинетики анодного растворения металлов широко применяются методы снятия поляризационных кривых и температурно-кинетический метод. Рассмотрим несколько примеров использования этих методов применительно к анодному растворению металлов и сплавов различной природы. [9]
Страницы: 1