Кинетика - реакция - восстановление
Cтраница 1
Кинетика реакций восстановления смешанными гидридами также еще до сих пор изучена очень мало, так что описание этих соединений здесь в известной мере отражает только последовательность их использования в практике. [1]
Проведенное нами экспериментальное исследование кинетики реакций восстановления окислов свинца и цинка окисью углерода [2, 3] с образованием жидкого и парообразного продуктов показало существенное отличие установленных кинетических закономерностей от характерных для процессов восстановления, протекающих с образованием твердых продуктов. [2]
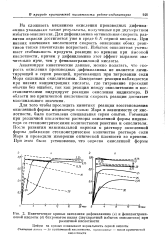 |
Кинетические кривые окисления дифениламина ( а и фенилантраниловой кислоты ( б бпхроматом калия ( двухкратный избыток окислителя при. [3] |
Для того чтобы проследить кинетику реакции восстановления окисленной формы индикатора солью Мора в зависимости от кислотности, была поставлена специальная серия опытов. [4]
Хаит и Сейджер [147] изучали кинетику реакции восстановления перхлорат-иона оловом ( II) в сернокислой среде и затем [148] использовали эту реакцию для определения перхлорат - и хлорат-ионов в присутствии друг друга, уточнив, что для этой цели предпочтительней в качестве восстановителя использовать цинк. [5]
Одним из самых интересных вопросов в кинетике реакций восстановления хрома ( У1) до хрома ( Ш) является вопрос о промежуточных степенях окисления. Как указывает Вестеймер [175], благодаря именно образованию этих реакционноспособных промежуточных соединений протекают многие индуцированные реакции хрома ( У1), невозможные с точки зрения термодинамических равновесных процессов. Так, например, Эспенсен [176] показал, что реакция между хромом ( У1) и ванади-ем ( 1У) индуцирует окисление иодида благодаря взаимодействию последнего с хромом ( У), образующимся в качестве промежуточного продукта в первичной реакции. [6]
Не менее интересные эффекты выявляются при исследовании кинетики реакции восстановления. Поскольку в реакции участвуют три компонента ( бихромат калия, сульфит натрия и серная кислота), было исследовано влияние на характер и скорость протекания реакции основных кинетических факторов: концентрации активных ионов водорода, исходной концентрации Сга и концентрации реагента в обезвреживаемом растворе. [7]
Лавровский с соавторами не изучали механизм и кинетику реакции восстановления окислов железа метаном, и отрицательные результаты их опытов следует отнести за счет неправильного выбора соотношения окислов железа и метана. [8]
В течение долгого времени основное внимание при изучении вопросов кинетики реакций восстановления было сосредоточено на реакции выделения молекулярного водорода, для которой был предложен ряд механизмов. Как легко убедиться, механизмы эти можно рассматривать как частные случаи тех, с которыми мы встречаемся при рассмотрении других реакций электровосстановления. [9]
При псевдоселективной коррозии коэффициент избирательного растворения Z резко меняет свои значения в зависимости от условий, определяющих кинетику реакции восстановления ионов благородного компонента. Последняя, прежде всего, зависит от перенапряжения. Интерметаллические фазы, где благородным компонентом является железо, кобальт или никель, не могут разрушаться по псевдоизбирательному механизму, так как потенциалы восстановления ионов этих металлов в кислых растворах не достижимы, а в нейтральных - трудно подобрать такой неблагородный компонент, который сообщил бы интерметаллической фазе необходимый потенциал. [10]
По Николаевой, Дамаскину и Акопяну 78, даже различие размеров одновалентных ионов в ряду щелочных металлов Cs - Li оказывает существенное влияние на плотность тока и, следовательно, на форму кривой. Кинетика реакции восстановления S20g - еще не выяснена. [11]
Такую запись нетрудно осуществить в статической системе, используя происходящее при протекании реакции изменение давления газа. Однако этот же принцип можно применить для изучения кинетики реакций восстановления в кипящем слое, если система, благодаря циркуляции газа, остается замкнутой. [12]
Сомов и Жуховицкий [54, 55] для исследования равновесий и кинетики гетерогенных процессов применили метод измерения микрообъемоз газа при помощи ионизационного детектора. Они определили термодинамические характеристики процесса диссоциации Ag2O и РЬО, а также изучили кинетику реакций низкотемпературного восстановления окислов ванадия, молибдена и железа. [13]
В работах Н. В. Николаевой-Федорович рассмотрено влияние адсорбированных ПАВ на реакции восстановления анионов и окисления катионов. Результаты, полученные в этих и некоторых других исследованиях, полностью подтверждают электростатический характер действия ПАВ на кинетику реакции восстановления. Рассматривая влияние Wi потенциала на скорость реакции, следует заметить, что основная часть ионов расположена во внешней плоскости Гельмгольца и в диффузном слое, однако имеется некоторое количество ионов, которые находятся во внутренней области Гельмгольца и непосредственно соприкасаются с поверхностью электрода. Было показано, что именно эти ионы и участвуют в разряде. [14]
Недавно изучался процесс фотовосстановления эозина Y аллил-тиомочевиной [34] - соединения, представляющего для нас особый интерес, так как оно участвует в целом ряде процессов биохимического восстановления. Аллилтиомочевина восстанавливает возбужденные молекулы эозина, не вызывая в то же время заметного падения интенсивности флуоресценции. Этот факт, а также довольно низкий квантовый выход реакции ( максимально 0 092) и данные о кинетике реакции восстановления указывают, что аллилтиомочевина реагирует с метастабильными формами, которые образуются из флуоресцентного ( синглетного) состояния, но не могут снова в него возвратиться. [15]
Страницы: 1 2