Кинетика - восстановление - водород
Cтраница 1
Кинетика восстановления водорода доводит рассмотрение вопроса до образования из ионов Н молекул EU. Последние должны покидать поверхность электрода, без чего не может установиться стационарное состояние. [1]
Я представляет кинетику восстановления водорода на никеле в том же растворе. Верхняя кривая несколько причудливой формы выражает изменение потенциала в зависимости от lg i при анодной поляризации никеля. Экстраполяция прямой Н до пересечения с анодной кривой ( точка А) дает логарифм плотности тока, отвечающего стационарному потенциалу окисления никеля ионами водорода в данном растворе. Этот потенциал принят за начало координат. [2]
Нижняя тафелев-ская прямая Я представляет кинетику восстановления водорода на никеле в том же растворе. Верхняя кривая несколько причудливой формы выражает изменение потенциала в зависимости от Igi при анодной поляризации никеля. Экстраполяция прямой Я до пересечения с анодной кривой ( точка А) дает логарифм плотности тока, отвечающего стационарному потенциалу окисления никеля ионами водорода в данном растворе. Этот потенциал принят за начало координат. [3]
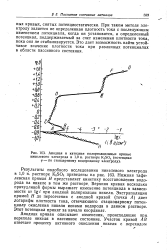 |
Анодная и катодная поляризационные кривые. [4] |
Нижняя тафе-левская прямая Н представляет кинетику восстановления водорода на никеле в том же растворе. Верхняя кривая несколько причудливой формы выражает изменение потенциала в зависимости от lg t при анодной поляризации никеля. Экстраполяция прямой Н до пересечения с анодной кривой ( точка А) дает логарифм плотности тока, отвечающего стационарному потенциалу окисления никеля ионами водорода в данном растворе. Этот потенциал принят за начало координат. [5]
И в этом случае стадия ( а), являясь более медленной, определяет кинетику восстановления водорода. [6]
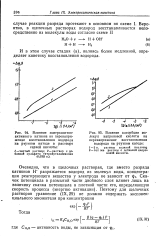 |
Влияние поверхностно-активного катиона на перенапряжение восстановления водорода на ртутном катоде в растворе.| Влияние адсорбции молекул капроновой кислоты на перенапряжение восстановления. [7] |
И в этом случае стадия ( а), являясь более медленной, определяет кинетику восстановления водорода. [8]
Чаще встречается коррозия сплавов. Поэтому величина г н на сплавах представляет особенно большой практический интерес. Однако кинетика восстановления водорода на сплавах исследована значительно менее полно, чем на чистых металлах. Если компоненты сплава имеют определенные величины а и Ъ, то каковы они будут на сплаве данного состава, хотя бы двухкомпонентном, мы пока предсказать не можем. [9]
Нужно иметь в виду, что исследование перенапряжения на ртутном катоде в щелочных растворах встречает значительные трудности. Сильно сдвинутый в отрицательную сторону равновесный потенциал водородного электрода в сочетании с большим перенапряжением приводит к тому, что совместно с восстановлением водорода начинается восстановление щелочных металлов, образующих амальгаму. Приходится принимать особые меры, чтобы выделить изучаемый процесс восстановления водорода. Поэтому данных для щелочных растворов имеется сравнительно мало. Тем не менее, рис. 96 подтверждает рядом точек влияние рН на перенапряжение в кислой области и хотя бы двумя точками - в щелочной. Подобное же уменьшение перенапряжения с ростом рН в щелочной области установлено для никелевого и платинового электродов. Но вообще кинетика восстановления водорода в щелочных растворах изучена менее подробно, чем в кислых. [10]
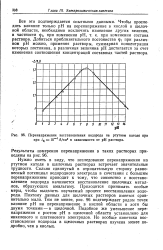 |
Перенапряжение восстановления водорода на ртутном катоде при при / IQ 10 - 4 А / см2 в зависимости от рН раствора. [11] |
Нужно иметь в виду, что исследование перенапряжения на ртутном катоде в щелочных растворах встречает значительные трудности. Сильно сдвинутый в отрицательную сторону равновесный потенциал водородного электрода в сочетании с большим перенапряжением приводит к тому, что совместно с восстановлением водорода начинается восстановление щелочных металлов, образующих амальгаму. Приходится принимать особые меры, чтобы выделить изучаемый процесс восстановления водорода. Поэтому данных для щелочных растворов имеется сравнительно мало. Тем не менее, рис. 96 подтверждает рядом точек влияние рН на перенапряжение в кислой области и хотя бы двумя точками - в щелочной. Подобное же уменьшение перенапряжения с ростом рН в щелочной области установлено для никелевого и платинового электродов. Но вообще кинетика восстановления водорода в щелочных растворах изучена менее подробно, чем в кислых. [12]
Страницы: 1