Кинетика - дегидрогенизация
Cтраница 2
Следует отметить, что многие проводившиеся до сих пор работы no - кинетике дегидрогенизации циклогексана и его производных не могли дать представления о механизме этой реакции хотя бы потому, что кинетика реакции дегидрогенизации не сопоставлялась с кинетикой возможных промежуточных реакций диспропорционирования. [16]
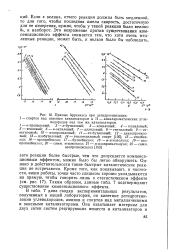 |
Прямые Аррениуса при дегидрогенизации. [17] |
В табл. 7 дана сводка экспериментальных результатов, полученных в нашей лаборатории, по кинетике дегидрогенизации углеводородов, аминов и спиртов над металлическими и окисными катализаторами. [18]
В данной статье об активных центрах катализаторов будут изложены некоторые новые выводы, к которым привели исследования кинетики дегидрогенизации. [19]
В статье А. А. Баландина рассматриваются выводы о природе активных центров на поверхности металлов и окислов, вытекающие из исследований кинетики дегидрогенизации и родственных реакций, проводимых автором и его сотрудниками. В статье описывается также применение стереохимии и метода меченых атомов к решению этих вопросов. С учетом адсорбции были найдены энергии активации и их зависимость от строения и ориентации молекул; построены модели активных центров и активных комплексов. Результаты кинетических исследований оказываются в хорошем согласии с мультиплетной теорией катализа, как в ее структурном, так и в ее энергетическом аспектах. [20]
Исключая члены, содержащие Р, и производя замену согласно ( г), мы получаем формулу ( III, 60), примененную А. А. Баландиным в статье [7] для расчеча кинетики дегидрогенизации бутилена в бутадиен. [21]
Исключая члены, содержащие Р, и производя замену согласно ( г), мы получаем формулу ( III, 60), примененную А. А. Баландиным в статье [7] для расчеча кинетики дегидрогенизации бутилена в бутядиен. [22]
Кинетика дегидрогенизации изопро-пилового спирта в присутствии меди, кобальта, никеля, железа, серебра, платины и палладия. [23]
Недавно появилось несколько работ Пшежецкого, Любарского, Щегловой и Мериляйнена [7] из Физико-химического института им. Карпова по кинетике дегидрогенизации бутана и бутилена. Положительном стороной этих работ является получение нового материала в этой области. [24]
Параметры решеток близки: для WSa а 3 18, с12 5 А, для MoSa а 3 15, с12 ЗОА. Над ними была изучена кинетика дегидрогенизации циклогексена и дегидрогенизации и дегидратации спиртов при 1 атм ( А. А. Толстопятова, автор, В. В отношении дегидрогенизации спирта MoS2 более активен, чем WS2, на WSs идет только дегидратация, а на MoS2, кроме того, и дегидрогенизация. [25]
Интересно, что в них для дегидрогенизации бутилена подтверждено наше кинетическое уравнение ( 1), но с другими коэффициентами вследствие другого состава катализатора - окись хрома с окисью алюминия. То же уравнение распространено и на кинетику дегидрогенизации бутана. [26]
 |
Модель активного комплекса при дублетной дегидрогенизации. Дегидрогенизация к-бутилового спирта на никеле. а - вид сверху. б - вид сбоку. [27] |
То же относится и к величинам относительных адсорбционных коэффициентов г продуктов реакции. Аналогичная закономерность была обнаружена также при исследовании кинетики дегидрогенизации ряда вторичных спиртов. Все данные получены на одном и том же образце окисного катализатора. [28]
Зелинский и А. А. Баландин исследовали кинетику каталитической дегидрогенизации декагидронафталина. Оказалось, что каталитическая дегидрогенизация этих углеводородов протекает очень гладко и подчиняется уравнению Аррениуса, что позволяет вычислить энергию активации этого процесса, составляющую 160ЭО - 19000 кал / моль для палладиевых и платиновых катализаторов, приготовленных различным образом. Методика изучения кинетики дегидрогенизации гидроароматических углеводородов, разработанная главным образом А. А. Баландиным, отличается большим совершенством, что позволило этой реакции стать одним из наиболее изученных гетерогенно-каталитических процессов в органической химии. Главные выводы упомянутых исследований послужили основой, на которой создалась мультиплетная теория катализа Баландина, являющаяся в настоящее время одной из руководящих теорий в этой области и с течением времени охватившая и объяснившая много новых фактов и явлений. [29]
Кистяковского с сотрудниками 53 по теп лотам гидрогенизации, что дегидрогенизация циклогексана с образованием промежуточных форм циклогексена и циклогексадиена невозможна по термодинамическим соображениям. Каган и Р. М. Фли д 55 на основании данных по кинетике дегидрогенизации циклогексана и метилциклогексана на палладиевом и хромовом катализаторах в присутствии акцептора водорода, в качестве которого брался ароматический углеводород, вновь высказали соображения в пользу того, что процесс дегидрирования циклогексана на любом катализаторе протекает ступенчато. Весьма любопытно, что, по данным этих авторов, энергия активации реакции дегидрогенизации циклогексана в условиях, когда свободный водород не выделяется, оказалась равной 10 000 кал / мол на палладии, нанесенном на силикагеле, и 13 000 кал / мол на окиси хрома, также нанесенной на силикагеле. [30]
Страницы: 1 2