Адсорбционная кинетика
Cтраница 1
Адсорбционная кинетика изучает процессы химического превращения с учетом явлений адсорбции, десорбции, хемосорбции. Скорость химической реакции зависит от концентрации реагентов в зоне реакции, следовательно, результирующая скорость процесса будет определяться процессом адсорбции. [1]
Многостадийные гетерогенные химические реакции изучаются диффузионной и адсорбционной кинетикой. В диффузионной кинетике исследуется влияние скорости диффузии реагентов на скорость реакции. В зависимости от соотношения скоростей реакции и диффузии различают три области протекания реакции: диффузионную, кинетическую и промежуточную. В диффузионной области лимитирующей является скорость диффузии реагентов. В кинетической области скорость химического превращения определяется скоростью реакции. В промежуточной области скорости диффузии и реакции соизмеримы. [2]
Здесь нужно упомянуть о другом подходе к адсорбционной кинетике, в котором не сделано попытки вывести уравнение скорости адсорбции и рассмотрены только небольшие отклонения от равновесия. Скорость адсорбции выражается в виде частных производных скорости относительно поверхностной и объемной концентраций, а также потенциала. Подробности здесь не приводятся, так как эта книга не рассматривает методики. Краткий обзор дан Парсонсом [6], а детали можно найти в работе Лоренца [66], который дал наиболее удовлетворительную трактовку этого вопроса. Следует также сослаться на работы Фрумкина и Мелик-Гайказяна [41, 67], которые первыми применили перемен-ноточную технику для изучения адсорбционной кинетики. Из результатов, полученных до сих пор, можно заключить, что адсорбция на ртути в водных растворах является быстрым процессом, который в основном контролируется диффузией. Лоренц [66] привел данные по определению скорости адсорбции для условий, соответствующих почти полному диффузионному контролю, и возникает вопрос, в действительности ли он измерил эффекты, относящиеся к относительно медленной адсорбции. [3]
Как уже отмечалось выше, простейшими в адсорбционной кинетике являются процессы, контролируемые или диффузией или собственно актом адсорбции. Определим критерии применимости для каждого из таких случаев. [4]
Следует подчеркнуть, что приближенность оценки отнюдь не ухудшает критериев диффузионной и адсорбционной кинетики, полученных на этой основе, поскольку указанные критерии выражаются усиленными неравенствами или, лишь в таком виде и позволяющими существенно упростить исходные уравнения. В случае же смешанной кинетики ( когда эти неравенства не выполняются) все равно приходится пользоваться исходными уравнениями, так что знание точного соотношения вкладов от различных механизмов адсорбции не представляет, по-видимому, никакой практической ценности. [5]
В соответствии с формулами ( 23), ( 73), ( 76) критерии чисто адсорбционной кинетики для больших ( по сравнению с молекулами растворителя) молекул ПАВ произвольной формы совпадают с критериями ( 53) - ( 55), полученными для молекул сравнимых размеров. [6]
Кинетика заторможенного добавками N0 или пропилена распада пропана, согласно выше изложенной теории, представляет один из вариантов адсорбционной кинетики, определяемой конкурентными адсорбционными отношениями ингибитора и алкана. [7]
При изучении двойного слоя всегда подчеркиваются его равновесные свойства, и была сделана только одна попытка найти общее уравнение скорости для адсорбционной кинетики. [8]
Из этого неравенства следует, что правая часть неравенства ( 132) в этих условиях всегда много меньше единицы. Таким образом, для чисто адсорбционной кинетики адсорбции условие ( 132) практически всегда выполняется, если в системе имеется растворимое ПАВ. [9]
Более полное рассмотрение для случая чисто адсорбционной кинетики было дано в работе [ 37, с. [10]
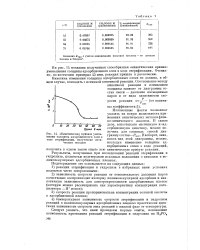 |
Кинетическая кривая уменьшения толщины адсорбционного слоя в ходе этерификации, полученная оптическим методом. [11] |
Изложенные факты позволяют указать на новую возможность применения кинетических методов физико-химического анализа. В самом деле, сопоставляя истинную и адсорбционную кинетику, можно получить для сложных смесей диаграмму состав - Рнас. Наоборот, зная, каков вид этой диаграммы, можно, исследуя изменение толщины адсорбционных слоев в ходе реакций, получить в одном таком опыте всю кинетическую кривую реакции. [12]
Здесь нужно упомянуть о другом подходе к адсорбционной кинетике, в котором не сделано попытки вывести уравнение скорости адсорбции и рассмотрены только небольшие отклонения от равновесия. Скорость адсорбции выражается в виде частных производных скорости относительно поверхностной и объемной концентраций, а также потенциала. Подробности здесь не приводятся, так как эта книга не рассматривает методики. Краткий обзор дан Парсонсом [6], а детали можно найти в работе Лоренца [66], который дал наиболее удовлетворительную трактовку этого вопроса. Следует также сослаться на работы Фрумкина и Мелик-Гайказяна [41, 67], которые первыми применили перемен-ноточную технику для изучения адсорбционной кинетики. Из результатов, полученных до сих пор, можно заключить, что адсорбция на ртути в водных растворах является быстрым процессом, который в основном контролируется диффузией. Лоренц [66] привел данные по определению скорости адсорбции для условий, соответствующих почти полному диффузионному контролю, и возникает вопрос, в действительности ли он измерил эффекты, относящиеся к относительно медленной адсорбции. [13]
Страницы: 1