Формальная кинетика
Cтраница 1
Формальная кинетика изучает зависимость скорости реакции ( протекающей при постоянной температуре) от различных факторов, а также занимается классификацией химических реакций. Формальная кинетика не объясняет характера наблюдаемых зависимостей и детального механизма протекающих процессов. Процессы изучаются и классифицируются на основе нескольких принципов, принимаемых за аксиомы. К их числу относится закон действующих масс, который позволяет выразить скорость химической реакции с помощью молярных концентраций реагентов. [1]
Формальная кинетика описывает химический процесс без глубокого изучения механизма реакций. Она базируется на формальном применении закона действующих масс для описания ско - рости не только элементарных, но и для простых и сложных реакций. Тем не менее формальные кинетические уравнения, благодаря простоте, находят широкое применение в инженерных расчетах и кинетических исследованиях. [2]
Формальная кинетика описывает химический процесс без глубокого изучения механизма реакций. Она базируется на формальном применении закона действующих масс для описания скорости не только элементарных, но и для простых и сложных реакций. Тем не менее формальные кинетические уравнения, благодаря простоте, находят широкое применение в инженерных расчетах и кинетических исследованиях. [3]
Формальная кинетика изучает зависимость скорости реакции ( протекающей при постоянной температуре) от различных факторов, а также занимается классификацией химических реакций. Формальная кинетика не объясняет характера наблюдаемых зависимостей и детального механизма протекающих процессов. Процессы изучаются и классифицируются на основе нескольких принципов, принимаемых за аксиомы. К их числу относится закон действующих масс, который позволяет выразить скорость химической реакции с помощью молярных концентраций реагентов. [4]
Формальная кинетика рассматривает процесс, не интересуясь механизмом реакции, чисто количественно описывает результат всех стадий, всех превращений, результат всей реакции в целом. Для этого необходимо определить порядок реакции по отношению к каждому из реагирующих веществ, составить дифференциальное уравнение для скорости реакции и проинтегрировать его. Составление дифференциального кинетического уравнения - задача физико-химическая, требующая знания порядка реакции. Интегрирование дифференциального уравнения - задача чисто математическая. [5]
Формальная кинетика рассматривает процесс реакции в целом, не интересуясь ее истинным механизмом: дает чисто количественное описание результата взаимодействия частиц, не изучая деталей этого процесса. Теория Аррениуса позволяет вычислить энергию активации для реакции в целом, но не отвечает на вопрос о том, что представляет собой эта энергия, как она связана с механизмом реакции и строением молекул. [6]
Формальная кинетика ферментативных реакций основывается на теории Михээлиса - Ментен [ 298, И. [7]
Формальная кинетика выделения летучих веществ была недавно рассмотрена в нескольких работах, в частности в обширной области скоростей нагрева. [8]
Формальная кинетика параллельных и последовательных реакций является, естественно, более сложной, чем кинетика простых реакций. [9]
Формальной кинетикой называется раздел химической кинетики, в котором рассматривается количественное описание хода химической реакции во времени при постоянной температуре в зависимости от концентрации реагирующих веществ. Знание кинетических характеристик химических процессов имеет большое практическое и теоретическое значение, так как позволяет рассчитывать реакторы и различную химическую аппаратуру и находить наиболее общие методы выяснения механизма реакции, открывая пути для сознательного управления и совершенствования существующих и создания новых технологических процессов. [10]
Изучена формальная кинетика реакции эпоксидирования 4 - ВЦГ ГПТБ в присутствии тетрабутоксититана. Порядок реакции по каждому компоненту близок к единице. Определена энергия активации, которая составила 69 9 кДж / моль. [11]
Уравнения формальной кинетики корректны в ограниченной области изменения параметров технологического процесса, достаточной для решения задач оптимизации и автоматического управления. [12]
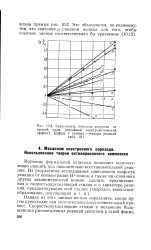 |
Зависимость констант скорости от. [13] |
Изучение формальной кинетики позволяет количественно описать ход окислительно-восстановительной реакции. [14]
Методы формальной кинетики, описанные в гл. IX, позволяют вычислять некоторые индивидуальные константы скорости мономолекулярных стадий - и константы равновесия для некоторых бимолекулярных стадий ферментативной реакции. Ниже мы обсудим стратегию и тактику, применяемые для этих целей. В следующих главах будет показано, как можно использовать эти константы для выявления важных функциональных групп в молекуле фермента и установления их роли в катализе. [15]
Страницы: 1 2 3 4