Кипение - серная кислота
Cтраница 1
Кипение серной кислоты все-время должно быть слабым. Сильное кипение ведет к потере азота вследствие частичного разложения сульфата аммония. [1]
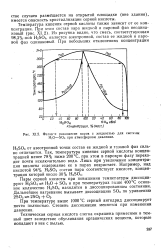 |
Фазовое равновесие паров с жидкостью для системы Н2О - SO3 при атмосферном давлении. [2] |
Температура кипения серной кислоты также зависит от ее концентрации. При этом состав пара жидкой и паровой фаз неодинаковый ( рис. XI. Из рисунка видно, что смесь, соответствующая 98 3 % - ной H2SO4, является азеотропной, состав ее жидкой и паровой фаз одинаковый. [3]
 |
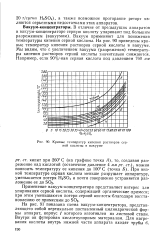
Зависимость температуры кипения серной кислоты и содержания H2SO в парах от содержа -, ния H2SO4 в растворе. [4] |
Температура кипения серной кислоты g увеличением ее концентрации повышается. Вначале при кипении слабой серной кислоты до содержания в ней 70 % H2SO4 в пары переходит только вода. [5]
Поскольку точка кипения серной кислоты очень высока, все ее количество, содержащееся в растворителе, остается после перегонки в колбе в виде отстоя. Иными словами: если, например, после Перегонки 100 мл раствора остается 1 мг отстоя, то вся содержавшаяся в этом количестве растворителя серная кислота будет сосредоточена в отстое. Поэтому целесообразно определять наличие в растворителе серной кислоты, подвергая исследованию именно его отстой. [6]
 |
Схема сульфирования бензола в парах. [7] |
При нагревании до кипения серной кислоты ( содержащей воду) и бензола пары последнего уносят воду, повышают концентрацию кислоты до начала сульфирования, а затем, уводя постепенно реакционную воду, дают возможность использовать до конца серную кислоту. [8]
Как меняется точка кипения серной кислоты от ее крепости. [9]
Так, температура кипения серной кислоты концентрацией менее 78 % ниже 200 С, при этом в паровую фазу переходит почти исключительно вода. Лишь при увеличении концентрации кислоты содержание ее в парах возрастает. [10]
Как изменяется температура кипения серной кислоты в зависимости от ее концентрации. [11]
Уделыбле теплоемкости и температуры кипения серной кислоты приведены. [12]
Сравнительно невысокие температуры плавления и кипения серной кислоты, а также ее большая растворимость в воде объясняются полярностью ее молекул. [13]
Так, при нагревании до кипения серной кислоты ( содержащей воду) повышают концентра - цию кислоты до начала сульфирования, при этом пары воды удаляются с парами вещества, в виде азеотропа, перегретого до 250 ( бензола), подвергающегося сульфированию. [14]
 |
Кривые температур кипения растворов серной кислоты в вакууме. [15] |
Страницы: 1 2 3 4