Кипение - вещество
Cтраница 4
В большинстве случаев температурой кипения вещества считают интервал температуры кипения, наблюдаемый при перегонке вещества. При этом могут возникнуть ошибки, связанные с перегревом паров и недостатками прибора ( например, неправильное положение термометра, см. стр. Дальнейшими источниками ошибок служат неточное исправление показаний термометра ( см. стр. Поэтому в литературе часто для одного и того же вещества встречаются различные значения температуры кипения. [46]
Для выполнения расчетов температуры кипения веществ при нестандартных давлениях по модели (5.18) требуется лишь информация о температурных и барических константах при фазовых их превращениях. В ней нет ни одного неизвестного коэффициента, следовательно, она является универсальной применимой для всех молекулярных веществ, в т.ч. углеводородов. [47]
В большинстве случаев температурой кипения вещества считают интервал температуры кипения, наблюдаемый при перегонке вещества. При этом могут возникнуть ошибки, связанные с перегревом паров и недостатками прибора ( например, неправильное положение термометра, см. стр. Дальнейшими источниками ошибок служат неточное исправление показаний термометра ( см. стр. Поэтому в литературе часто для одного и того же вещества встречаются различные значения температуры кипения. [48]
Однако весьма высокая точка кипения вещества заставляет нас воздержаться от придания ему определенного строения как изомера дитиолэтанфосфористой кислоты. [49]
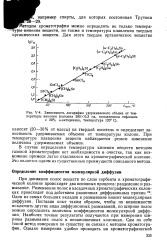 |
Зависимость логарифма удерживаемого объема от температуры кипения ( колонна 200X0 3 см, наполненная тефлоном с 20 % н-октадекана, температура 120е С. [50] |
В случае определения температуры кипения веществ методом газовой хроматографии нет необходимости в очистке, так как возможные примеси легко отделяются на хроматографическои колонне. Это является одним из существенных преимуществ описанного метода. [51]
Для выполнения расчетов температуры кипения веществ при нестандартных давлениях по модели (5.2) требуется лишь информация о температурных и барических константах при фазовых их превращениях. В ней нет ни одного неизвестного коэффициента, следовательно, она является универсальной и применимой для всех молекулярных веществ, в т.ч. углеводородов. [52]
В зависимости от точки кипения озонируемого вещества или применяемого растворителя, а также в зависимости от того, насколько опасны получаемые озониды, реакционные сосуды охлаждают водой, льдом, смесью льда и соли или смесью эфира и двуокиси углерода. [53]
Известно, что при кипении вещества при постоянном давлении поглощается тепло без изменения температуры. Эта удельная теплота испарения I ( измеряемая в калориях на г испаренного вещества), представляет собой разность кинетических энергий молекул в жидком и газообразном состояниях; это энергия, затраченная на преодоление межмолекулярных сил притяжения жидкости при переходе из одной фазы в другую. [54]
Известно, что при кипении вещества при постоянном давлении поглощается тепло - без изменения температуры. Эта удельная теплота испарения I ( измеряемая в калориях на 1г испаренного вещества), представляет собой разность кинетических энергий молекул Е жидком и газообразном состояниях; это энергия, затраченная на преодоление межмолекулярных сил притяжения жидкости при переходе из одной фазы в другую. [55]
Гидроксильная группа изменяет и температуру кипения вещества. Ее электрические свойства таковы, что содержащие ее молекулы слегка слипаются друг с другом. А молекулы жидкого метана, не содержащие гидроксиль-ных групп, не слипаются. Они легко разлетаются, образуя газ. Даже при такой низкой температуре, как - 161 С, тепла хватает, чтобы испарить метан - его температура кипения как раз - 161 С. А молекулы метилового спирта содержат гидроксильные группы, которые делают их липкими. Чтобы отделить их друг от друга и превратить в газ, нужно затратить немало энергии, хотя сами молекулы лишь немногим крупнее молекул метана. Вот почему температура кипения метилового спирта 65 С - на 226 градусов выше, чем у метана. [56]
 |
Номограмма для определения температуры кипения веществ при пониженном давлении. [57] |
При отсутствии литературных данных температуру кипения вещества в вакууме находят с помощью номограммы ( рис. 76) на продолжения прямой линии, соединяющей температуру кипения этого вещества при атмосферном давлении и значение остаточного давления. [58]
Скорость испарения зависит от температуры кипения веществ. Наибольшей испаряемостью обладают жидкости с низкими температурами кипения. [59]
Страницы: 1 2 3 4