Кислород - вода
Cтраница 3
В противоположность Траубе, Виланд допускает, что окисление кислородом воды происходит не через расщепление молекулы воды и связывание гидроксильных ионов, но через присоединение целых молекул воды и последующее дегидрирование возникающего гидрата. [31]
Известно, что кислород перекиси водорода не обменивается с кислородом воды. Так как разложение Н202 велось при температуре около 0 С, то был изучен обмен KJ03 с водой при этой температуре. [32]
Ингибиторы, адсорбирующиеся химически или способствующие окислению поверхности металла кислородом воды, сильно замедляют анодную реакцию ионизации металла и поэтому оказываются более эффективными, чем физически адсорбированные ингибиторы или ингибиторы, которые тормозят лишь одну катодную реакцию. [33]
При растворении в воде димер А12С16 распадается, так как кислород воды за счет своих неподеленных пар образует более прочные координационные связи с металлами, чей хлор. Такой же состав имеют и кристаллогидраты, выделяемые из водных растворов хлорида алюминия. [34]
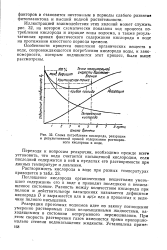 |
Слема потребления кислорода, реаэрации и результативной кривой содержания растворенного кислорода в воде. [35] |
Особенности процесса окисления органических веществ в воде, сопровождающегося потребления кислорода воды, и закономерности, которым подчиняется этот процесс, были выше рассмотрены. [36]
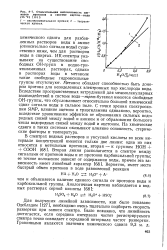 |
Относительная интенсивность сигналов протонов в системе ацетон-вода ( 25 С. [37] |
Метанол обладает способностью быть донором протона для неподеленных электронных пар кислорода воды. Вследствие пространственных затруднений для межмолекулярных взаимодействий в системе вода-трет-бутанол имеются свободные ОН-группы, что обусловливает относительно большой химический сдвиг сигнала воды в сильное поле. С точки зрения спектроскопии ЯМР, влияние ацетона и триэтиламина одинаково, вероятно, вследствие уравнивания эффектов от образования сильных водородных связей между водой и амином и от образования большого числа водородных связей между водой и ацетоном. На химические сдвиги в таких системах оказывают влияние основность, стериче-ские факторы и температура. [38]
Биохимическое потребление кислорода разбавляющей воды учитывается при вычислении биохимического потребления кислорода испытываемой воды. [39]
В таких системах применение хрома, обладающего оптимальным сродством к кислороду воды, затрудняет образование индивидуальных оксидных соединений в пассивирующем слое и повышает степень окисленности основного компонента сплава. Формируется смешанный оксид на основе хрома, легированный другими компонентами сплава, обладающий повышенной защитной способностью. Прочность связи кислорода в смешанных оксидах должна возрастать. [40]
Известно, что кислород гидроксильных групп спиртов не обменивается с кислородом воды. В этом соединении метоксильные группы, отталкивая электроны, способствуют проявлению основных свойств и ионизации гидроксила. Соединения кремния проявляют тенденцию к реакциям нуклеофильного замещения, являющуюся следствием электроположительного характера кремния. Мы предположили, что эта тенденция в силанолах может привести к кислородному обмену. Обмен путем нуклеофильного замещения обычно идет через промежуточный комплекс, образующийся при взаимодействии гидроксила или воды с положительным углеродом или иным центральным атомом. В спиртах, в противоположность карбонильным и карбоксильным соединениям, положительный характер углерода выражен слабо, что объясняет затрудненность кислородного обмена в гидроксиле. В силанолах положительный характер кремния, являющийся следствием значительной поляризации Si-ОН-связи, выражен достаточно сильно для возможности обмена путем нуклеофильного замещения. [41]
При заряде химические реакции идут в обратном направлении, при этом кислород воды расходуется на образование перекиси свинца на положительной пластине, а кислотный остаток сернокислого свинца обеих пластин и водород воды идут на образование серной кислоты в электролите. При дальнейшем пропускании тока происходит только разложение воды на кислород и водород, выделяющиеся из электролита в виде пузырьков. [42]
При заряде химические реакции идут в обратном направлении, при этом кислород воды расходуется на образование перекиси свинца на положительной пластине, а кислотный остаток сернокислого свинца обеих пластин и водород воды идут на образование серной кислоты в электролите. [43]
Поэтому перенос кислорода от воды не изменяет содержания О18, и кислород воды и сульфата имеет одинаковый состав, а перенос кислорода непосредственно от окислителя уменьшает долю О18 в сульфате. Результаты опыто з были выражены числом п атомов кислорода, отданных сульфату молекулой окислителя, найденным по уменьшению доли О18 в сульфате. Во всех случаях с окислителями ClOjj, СЮз BrOjj - и МпО2 найдены для п величины, близкие к стехиометрическим для непосредственного переноса без участил воды, но меньшие, чем последние. [44]
Существенным недостатком деаэраторов с перегревом воды является также необходимость пропуска содержащей кислород высокоподогретой воды через поверхностный подогреватель. Во избежание корродирования подогревателя для изготовления его приходится применять латунь или нержавеющую сталь, что, естественно, удорожит деаэратор. [45]
Страницы: 1 2 3 4