Элементарный кислород
Cтраница 1
Элементарный кислород может выделяться при электролизе или из самого эфира или из воды, присутствующей во фтористом водороде. [1]
Хотя элементарный кислород обычно довольно мало реакцион-носпособен, все же в реакциях аутоокисления он может затрагивать и трудно гомолизуемые С - Н - связи. [2]
Стандартная энтальпия элементарного кислорода равна нулю. [3]
При действии элементарного кислорода соединения типа R3T1 претерпевают окисление. [4]
Объясните, почему элементарный кислород химически реакционноспо-собен, в то время как элементарный азот инертен, с точки зрения их электронной структуры. [5]
Известно, что окисление элементарным кислородом хорошо очищенных углеводородов предельного характера протекает крайне трудно и медленно. Путем предварительного нагрева или добавки продукта, уже находившегося в данной реакции, окисление тех же углеводородов может быть значительно ускорено. Таким образом, ясно, что для начала нормального течения реакции окисления элементарным кислородом необходимо создание в среде углеводорода активных центров, в которых процесс мог бы получить свое начальное развитие. [6]
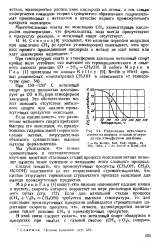 |
Разложение метилового спирта на водород и окись углерода при атмосферном давлении. [7] |
Многочисленные опыты по окислению СН4 элементарным кислородом подтверждают, что формальдегид, вода всегда присутствуют в продуктах реакции, а метиловый спирт отсутствует. [8]
В литературе описаны люминесцентные методы определения элементарного кислорода, озона и перекиси водорода. Для определения кислорода и озона обычно пользуются явлением возникновения или гашения флуоресценции органических красителей в результате их окисления. Так, например, было предложено387 определять кислород в щелочном растворе лейкооснования флуо-ресцеина ( флуоресцин), который получают восстановлением флуо-ресцеина в щелочном растворе цинковой пылью. Полученный флуоресцин не флуоресцирует в ультрафиолетовом свете; однако при пропускании через его щелочной раствор анализируемого газа следы кислорода приводят к возникновению флуоресцеина и по интенсивности флуоресценции раствора можно судить о количестве поглощенного раствором кислорода. [9]
В литературе описаны люминесцентные методы определения элементарного кислорода, озона и перекиси водорода. Для определения кислорода и озона обычно пользуются явлением возникновения или гашения флуоресценции органических красителей в результате их окисления. Так, например, было предложено387 определять кислород в щелочном растворе лейкооснования флуо-ресцеина ( флуоресцин), который получают восстановлением флуо-ресцеина в щелочном растворе цинковой пылью. Полученный флуоресцин не флуоресцирует в ультрафиолетовом свете; однако при пропускании через его щелочной раствор анализируемого газа следы кислорода приводят к возникновению флуоресцеина и по интенсивности флуоресценции раствора можно судить о количестве поглощенного раствором кислорода. [10]
В этих процессах в качестве реагента используют элементарный кислород ( или агенты окисления, которые выделяют кислород); в других случаях кислород может быть введен в молекулу при помощи, например, марганцовой и осмиевой кислот, ионов НО или свободных гидроксильных радикалов ( НО -) и другими методами. [11]
Реакции аутоокисления - это взаимодействия органических соединений с элементарным кислородом, приводящие к образованию гидроперекисных ROOH и перекисных ROOR соединений. Подобные превращения часто ускоряются продуктами реакции ( аутокатализ), отсюда и название - аутоокисление. [12]
Известно, что ряд вторичных спиртов легко окисляется элементарным кислородом, давая с хорошим выходом кетоны и перекись водорода. Мы вели эту реакцию с 3 2 г спирта, перегнанного в эвакуированную ампулу иэ молибденового стекла, которая была предварительно длительно обработана раствором борной кислоты и пергидролем. Изотопный состав ее приведен в таблице. В этом случае также весь кислород перекиси водорода происходит из элементарного кислорода без участия кислорода из спиртового гидроксила. [13]
Значительно более сложным является вопрос о механизме окисления элементарным кислородом углеводородов и боковых цепей предельного характера. Приходится констатировать, что полного единства во взглядах здесь еще не достигнуто, и в последующем изложении мы вкратце рассмотрим две основных точки зрения на этот сложный химический процесс. [14]
Следует обратить внимание на повышенную чувствительность смолистых веществ к элементарному кислороду. Андреева получить бескислородные смолы при термокатализе чистых метаново-нафтеновых углеводородов, в условиях максимального предохранения от воздействия воздуха, не достигли цели. [15]
Страницы: 1 2 3