Атмосферный кислород
Cтраница 3
Первая гипотеза о происхождении атмосферного кислорода была фактически выдвинута самим Пристли. Вспомним, что, поместив однажды ветвь растения в воздух, испорченный в результате длительного пребывания в нем мыши настолько, что мышь погибла, Пристли через несколько дней убедился, что воздух возвратил свои первоначальные свойства поддерживать горение и дыхание. [31]
Согласно биохимической теории возникновения атмосферного кислорода первоисточником его является, следовательно, углекислый газ, а превращение последнего в кислород есть результат деятельности растительного мира минувших геологических эпох. Из этой гипотезы вытекает с очевидностью доступное проверке следствие: запас кислорода в атмосфере земного шара должен быть химически эквивалентен запасу в нем органической материи, включая органические вещества, захороненные в недрах земли в виде каменного угля, нефти и нефтяных газов. [32]
В настоящее время объем атмосферного кислорода уменьшается на 10 млрд. т в год, а 40 % речного стока вод идет на потребление и по некоторым прогнозам к концу века ресурсы чистых пресных вод могут оказаться исчерпанными. Накопление углекислого газа в атмосфере при сжигании топлива идет более интенсивно, чем его поглощение растительностью и водами океанов и морей. [33]
Вредные последствия окисления полимеров атмосферным кислородом экономически особенно существенны при использовании натурального и большинства синтетических каучуков. Выяснение ( примерно 20 лет назад) роли кислорода в процессах, приводящих к ухудшению свойств резиновых изделий, привело к применению антиокислителей, значительно увеличивающих срок службы этих изделий. По аналогии с простейшими соединениями можно сделать вывод, что присутствие двойных связей до некоторой степени обусловливает высокую реакционную способность ненасыщенных полимеров по отношению к кислороду. В течение последних 60 - 70 лет были высказаны различные предположения о природе реакции между кислородом и олефино-вым соединением. Однако удовлетворительное объяснение было дано только сравнительно недавно, главным образом в результате работ по исследованию реакций больших молекул того или иного типа. [34]
 |
Зависимость степени извлечения от рН для экстракции некоторых тиооксинатов металлов в хлороформ. [35] |
Этот реагент легко окисляется атмосферным кислородом с образованием дисульфида. [36]
Этот реагент легко окисляется атмосферным кислородом как в водных растворах, так и в растворах в органических растворителях с образованием дисульфида; в связи с этим его часто используют в виде цинковой соли. Затем в реакционной - смеси реагент выделяют в свободном состоянии действием кислоты или щелочи. Его успешно применяют для экстракционного разделения и фотометрического определения молибдена в присутствии вольфрама. Молибден может экстрагироваться яз 6 - 14 М растворов серной кислоты или 3 7 М раствора соляной кислоты. [37]
Окисные пленки, создаваемые атмосферным кислородом, непрочны, образование их происходит стихийно и не поддается контролю, они не защищают от микроизноса; наоборот, интенсивное формирование таких пленок влечет за собой быстрое истирание поверхности. Коэффициенты трения их высоки. [38]
Реакции окисления, в которых атмосферный кислород реагирует с горючими газами и парами, настолько хорошо известны и часто протекают так быстро, что, естественно, возникает тенденция рассматривать молекулу кислорода как весьма реакционно-способную. Цепные реакции протекают также и при медленном окислении насыщенных, ненасыщенных углеводородов, их производных и некоторых неорганических веществ как в растворах, так и в чистых жидкостях. Цепной характер этих автоокислительных реакций был впервые установлен Бэкстремом путем сравнения фотохимического и термического окисления альдегидов и сульфита натрия ( см. стр. Подобно всем цепным реакциям, скорости этих реакций можно увеличить, добавляя катализаторы, дающие соответствующие свободные радикалы при термическом или фотохимическом разложении или за счет реакции переноса электрона; их скорости можно уменьшить введением ингибиторов, которые заменяют активные радикалы неактивными или молекулами. Некатализируемые реакции автоокисления обычно идут медленно, потому что медленной является начальная стадия взаимодействия между реагентами, приводящая к образованию свободных радикалов. Однако при некоторых обстоятельствах реакции автоокисления обнаруживают самоускорение или автокатализ, обусловленный бирадикальными свойствами молекулы или атома кислорода. Поэтому представляет интерес рассмотреть некоторые общие особенности реакций автоокисления в связи с реакционно-способностью молекулы кислорода. [39]
В атомных реакторах не расходуется атмосферный кислород. На современных атомных электростанциях практически полностью отсутствуют выбросы радиоактивных веществ, и концентрация радиоактивных аэрозолей в зоне АЭС ( радиусом 50 км) не превышает фоновых значений. [40]
Вулканизаты СКН хорошо сопротивляются действию атмосферного кислорода, озона и ультрафиолетовых лучей; по этим свойствам они превосходят натуральный каучук. Резины из СКН стойки к действию разбавленных растворов кислот и щелочей, а также растворов солей. Дивинил-нитрильные каучуки не растворяются в неполярных растворителях, в алифатических углеводородах, в нефтепродуктах ( бензине, керосине), но растворяются в полярных растворителях, например в кетонах. [41]
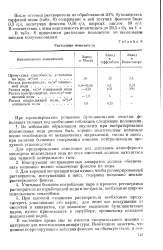 |
Расходные показатели. [42] |
Для предупреждения осмоления под действием атмосферного кислорода подсмольная вода во всех емкостях должна находиться под защитой нейтрального газа. [43]
Реакционную смесь необходимо защищать от атмосферного кислорода. При этом образуется прозрачный упругий нерастворимый гель, пригодный для электрофореза. Процесс идет без нагревания. В процессе полимеризации в геле образуются поперечные связи. Гели можно получать в присутствии различных буферных растворов, поэтому они пригодны к употреблению сразу после затвердевания. Смеси органических мономеров для приготовления геля выпускают фирмы American Cyanamid ( циагонам-41) и Е - С Apparatus Corp. Очистка материалов и приготовление геля описаны также в разделе, посвященном изоэлектрической фокусировке. [44]
Ниже 190 нм из-за поглощения атмосферного кислорода приходится использовать вакуумные УФ-спектрометры, причем известно лишь несколько примеров исследования матриц в области вакуумного ультрафиолета. Электронные переходы с энергией менее 12000 см 1 ( длина волны более 850 нм) наблюдаются редко, несмотря на то что активные частицы с неспаренными электронами и незанятыми орбиталями скорее должны иметь переходы с более низкой энергией, чем стабильные молекулы. Именно поэтому ближняя ИК-область ( 12000 - 3000 см 1), по-видимому, весьма интересна для матричных исследований. [45]
Страницы: 1 2 3 4