Исходный кислород
Cтраница 2
При автотермической конверсии задача несколько усложняется, поскольку при заданной температуре реакции искомый состав конвертированного газа также определяется соответствующим количеством исходного кислорода, который полностью вступает в реакцию. [16]
В Н202 были найдены те же самые процентные количества 180 - 180 и 180 - 160, как и в исходном кислороде. Отсюда однозначно вытекает, что связь О - О в молекуле О2 при восстановлении не рвется. [17]
При наличии ингибитора давление кислорода на верхнем пределе сильно понижается, и система оказывается в области, где гибель атомов кислорода при тройных соударениях значительно менее эффективна, чем их гибель при соударении с молекулами примеси, имеющейся в исходном кислороде. [18]
Марголис [143] изучен гемолитический обмен кислорода на металлах: серебре и платине, и на катализаторах полупроводниках: пятиокиси ванадия и двуокиси марганца. Исходный кислород содержал 24 % атомн. Реакционный объем откачивали до давления 10 - 6 мм рт. ст., затем в газовую форму вводили кислород, содержащий тяжелый изотоп кислорода О18 ( 15 % атомн. Это отношение является мерой гемолитического обмена кислорода на поверхности. В табл. 14 приведены данные о гемолитическом обмене кислорода на различных катализаторах. [19]
Однако значения бис, отвечающие экспериментальным данным, оказываются на несколько порядков больше, чем вычисленные теоретически. По-видимому, исходный кислород в опытах Тауша и Герлахера был недостаточно чист. [20]
Практически важно изучение влияния добавок азота, так как синтез озона часто проводят из воздуха. Наконец, известна зависимость эффективности синтеза от влажности исходного кислорода. Изучение синтеза озона из смесей кислород - аргон [111] показало, что добавки аргона снижают концентрацию озона, причем наблюдается линейная зависимость стационарной концентрации от состава смеси. [21]
Здесь мы опять сталкиваемся со случаем, когда чистота вещества определяет его стабильность. Находят, что если концентрация органических веществ в исходном кислороде ( в пересчете на углекислоту) ниже 20 частей на миллион, то из него можно получить стабильный 100 % - ный жидкий озон. [22]
Ожижеппую кислородную фракцию направляют в ректификационную колонну, нижняя часть, или пристройка, которой ( конденсатор) охлаждается жидким азотом. Здесь получается бедный криптоновый концентрат, содержащий 0 1 - 0 2 % Кг; этот бедняк в 400 раз богаче крип-топом, чем исходный кислород. [23]
Ожиженную кислородную фракцию направляют в ректификационную колонну, нижняя часть, или пристройка, которой ( конденсатор) охлаждается жидким азотом. Здесь получается бедный криптоновый концентрат, содержащий 0 1 - 0 2 % Кг; этот бедняк в 400 раз богаче криптоном, чем исходный кислород. [24]
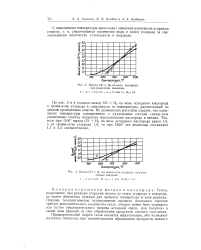 |
Выход СО На на моль кислорода.| Выход СО II на грамм-атом углерода при различном давлении. 1 - р - 15ати. II - р. ати. С Ог 1 9. [25] |
На рис. 3 и 4 показан выход СО Н2 на моль исходного кислорода и грамм-атом углерода в зависимости от температуры, рассчитанный по данным проведенных опытов. Из упомянутых рисунков следует, что повышение температуры одновременно с улучшением состава синтез-газа увеличивает степень полезного использования кислорода и метана. Так, если при 1100 выход СО Н2 на моль исходного кислорода равен 1 8, а на грамм-атом углерода 1 0, то при 1300 эти величины составляют 4 7 и 2 5 соответственно. [26]
Разумеется, криптон и ксенон - наименее летучие компоненты воздуха - скапливаются вместе с жидким кислородом в самой теплой части аппарата, откуда их и выделяют. Жидкий кислород подвергают ректификации, в результате чего получают бедный криптоновый концентрат, содержащий 0 1 - 0 2 % криптона и еще меньше ксенона. Впрочем, эпитет бедный здесь довольно относителен, если учесть, что концентрат в 400 раз богаче криптоном, чем исходный кислород. Прежде чем продолжить ректификацию, концентрат очищают от углеводородов, главным образом ацетилена и метана. Эта операция диктуется соображениями безопасности: ацетилен и метан, будучи растворенными в жидком кислороде, способны при известных условиях взрываться с огромной силой. Впервые взрыв кислородного аппарата произошел в 1908 г. вблизи Льежа ( Бельгия), в дальнейшем катастрофы случались и в других местах. Взрывы прекратились, как только была налажена очистка кислорода, а иногда и воздуха от углеводородов. [27]
Страницы: 1 2