Атомарный кислород
Cтраница 2
Атомарный кислород в момент выделения окисляет горючую жидкость, и последняя самовозгорается. [16]
Атомарный кислород особенно легко реагирует с разветвленными полимерами или с такими, которые содержат простые эфирные связи. [17]
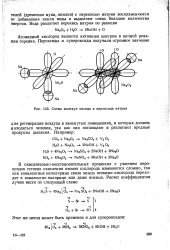 |
Схема молекул оксида и цероксида натрия. [18] |
Атомарный кислород является активным центром в цепной реакции горения. [19]
Атомарный кислород, азот и водород обладают большей активностью и интенсивнее растворяются в металле, ухудшая его свойства: снижают его пластичность и повышают хрупкость. [20]
Атомарный кислород может окислить ионы Сг3 до перекисей металлов, а Н2О2 окисляет ионы Сг3 в СгО42 в щелочном и нейтральном растворах, а в кислом растворе восстанавливает хроматы. [21]
Атомарный кислород обладает сильными окислительными свойствами, поэтому убивает микроорганизмы и окисляет органические примеси. [22]
Атомарный кислород, образующийся при разложении хлорной извести, оказывает и обеззараживающее действие. [23]
Атомарный кислород образует с топливом промежуточные соединения. [24]
Атомарный кислород и гндроксил, образующиеся при паровоздушном дутье, способны разорвать эту связь, в результате чего получается летучая моноокись германия, которая в дальнейшем может окислиться до двуокиси. Кроме того, атомарный кислород и гндроксил, вероятно, могут реагировать и с минеральными составляющими угля, выделяя в газовую фазу дополнительное количество летучих соединений германия по сравнению с количеством, выделяемым при горении топлива в воздушной среде. [25]
Атомарный кислород и азот активно вступают в реакции с металлом ( железом, марганцем и др.) и частично остаются в шве. Атомарный водород легко растворяется в жидкой стали и при ее затвердевании часто не успевает выделиться. [26]
Атомарный кислород существует в виде отдельных изолированных атомов с четным числом электронов. [27]
Атомарный кислород обладает особенно сильным окислительным свойством. Благодаря ему растворы пероксида водорода разрушают красящие вещества и отбеливают ткани из хлопчатобумажных и шерстяных тканей, шелк, перья, волосы. Способность пероксида водорода обесцвечивать волосы используют в косметике. Она основана на взаимодействии атомарного кислорода с красящим веществом волос меланином - смесью сложных органических веществ. При окислении меланин переходит в бесцветное соединение. Следует помнить, что пергидроль вызывает ожоги кожи и слизистых оболочек. [28]
 |
Кислородное дутье Равновесный состав. [29] |
Атомарный кислород образует с топливом промежуточные соединения. Универсальный характер этой закономерности справедлив для всех видов топлива. Далее будут показаны возможные промежуточные соединения при горении природного газа. Подчеркнем, что состав первичных продуктов горения зависит от структуры и химического строения промежуточного соединения. [30]
Страницы: 1 2 3 4