Фтористый кислород
Cтраница 1
Фтористый кислород, как и другие фториды кислорода, термодинамически неустойчив и легко распадается на простые вещества. Фториды кислорода мало полярны. [1]
Растворимость фтористого кислорода в 100 мл воды при 0 и 1 атм равна 6 8 мл. [2]
Фтор, фтористый кислород OF2, трехфтористый хлор C1F3, перхлоралфторид FC1O3, трехфтористый азот NF3 могут быть использованы в качестве окислителей в ракетном топливе. [3]
Растворим ость фтористого кислорода в 100 мл воды ори 0 и 1 атм равна 6 8 мл. [4]
Окислительные свойства и химическая активность фтористого кислорода выражены значительно слабее, чем у фтора. Хотя OF8 является эндотермическим соединением, оно не взрывает при пропускании искры. [5]
При более низкой концентрации щелочи образуется очень токсичный фтористый кислород. [6]
В последние годы интерес к изучению фтористого кислорода, а также ряда других соединений фтора ( например, C1O3F) объясняется возможностью их применения в качестве окислителей реактивного ракетного топлива. [7]
Как видно из этого уравнения, нитрат фтора является производным фтористого кислорода. В результате взаимодействия последнего со щелочью может выделяться и кислород. [8]
Естественно, что по своим свойствам NF3 резко отличается от взрывчатого хлористого азота и от фтористого кислорода. Трехфтористый азот не реагирует с водой или растворами щелочей, хотя эти процессы сильно экзотермичны. Гидролиз его паром воды протекает медленно. Смеси NF3 с Н2, H2S, СН4 и СО воспламеняются только при нагревании; в таких же условиях реагируют щелЪчные и щелочноземельные металлы, олово, медь и ртуть. [9]
Возможно, что эти старые указания ошибочны и примесь, принимавшаяся за озон, является фтористым кислородом. [10]
 |
Строение электронной оболочки невозбужденного атома хлора. [11] |
Как уже было упомянуто ранее, фтор является наиболее электроотрицательным элементом, поэтому все бинарные соединения со фтором являются фторидами, в частности OF2 является фторидом кислорода, и в этом соединении, конечно, фтор имеет сТсиень окисления - I, а кислород 11, из-за чего фтористый кислород является сильным окислителем. [12]
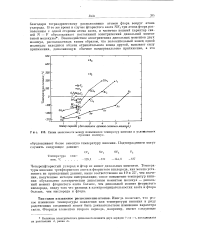 |
Схема зависимости между повышением температур кипения и усложнением. [13] |
Четырехфтористый углерод и фтор не имеют дипольных моментов. Температуры кипения трехфтористого азота и фтористого кислорода, как можно установить из приведенных данных, выше соответственно на 19 и 22, чем значения, полученные методом интерполяции; такое повышение температур кипения обусловлено электрическим дипольным моментом молекул - дипольный момент фтористого азота больше, чем дипольный момент фтористого кислорода, ввиду того что разница в электроотрицательностях азота и фтора больше, чем кислорода и фтора. [14]
 |
Стехиометрические коэффициенты активности плавиковой кислоты. [15] |
Страницы: 1 2