Чистая хлорная кислота
Cтраница 1
Чистая хлорная кислота кратковременно ( 3 - 5 недель) не взрывоопасна при хранении в темноте и при низких температурах. При температуре около 298 К ( 25 С) она может храниться не более месяца, и затем обычно взрывается. В процессе хранения образуется окись хлора ( С О) - очень нестойкое вещество, склонное к саморазложению и взрыву. [1]
Безводная чистая хлорная кислота представляет бесцветную жидкость с уд. Она не перегоняется без разложения при атмосферном давлении. При температуре около 90 начинается ее бурное разложение. Без разложения хлорная кислота перегоняется лишь в вакууме. [2]
Устойчивость чистой хлорной кислоты в процессе хранения может быть обеспечена путем периодической вакуум-перегонки или добавки стабилизатора 1 0 - 1 5 % - го четыреххлористого углерода. Стабилизированная хлорная кислота довольно устойчива. [3]
Никель пассивен в чистой хлорной кислоте, но в присутствии ионов ртути, разрушающих окисную пленку, окисляется ионами водорода и ионами ртути. [4]
Плотность системы по мере перехода от чистой хлорной кислоты к чистой уксусной кислоте равномерно уменьшается. [5]
Водные растворы хлорной кислоты более устойчивы, чем чистая хлорная кислота. С водой хлорная кислота образует кристаллы моногидрата НС1О4 - Н2О, или точнее Н3О С1О -, характерным свойством которых является высокая температура плавления ( 50; см. стр. [6]
Является одной из наиболее распространенных в химических лабораториях кислот, применяемых для разложения минералов, сплавов и др. Свободная чистая хлорная кислота дымит на воздухе, является сильным окислителем. С большинством органических соединений реагирует воспламеняясь или взрываясь, например, с деревом, бумагой, хлопчатобумажной тканью и пр. С водой смешивается во всех отношениях, образуя ряд гидратов. В чистом виде опасна, поэтому чаще применяют ее водные растворы. Соли ее - перхлораты идут для приготовления взрывчатых соединений и пиротехнических составов. Перхлорат магния в лабораториях применяют как хороший осушитель. Перхлораты не менее опасны, чем хлорная кислота. [7]
 |
Коивые анодной поляризации никеля в растворе 1 М НС1О4. [8] |
Так, для никеля в растворах НС1С4, по данным, представленным на рис. 37, видно, что в чистой хлорной кислоте на анодной поляризационной кривой обнаруживается один максимум тока при потенциале, близком к 0 1 в. Введение серной кислоты приводит к тому, что после начала первичной пассивации наблюдается временное активирование растворения, после которого вновь происходит пассивация. [9]
В качестве препарата кобальта применялся Со ( С1О4) 2 6Н2О, полученный из химически чистого, свободного от никеля, карбоната кобальта и химически чистой хлорной кислоты. [10]
Самовоспламенение иногда происходит весьма энергично и со взрывом. Чистая хлорная кислота не является вполне однородным веществом. В равновесном состоянии она содержит некоторое количество хлорного ангидрида и воды, связанных в гидрат хлорной кислоты. [11]
В отличие от остальных кислородсодержащих кислот хлора хлорная кислота НСЮ4 может быть получена в виде индивидуального вещества. Чистая хлорная кислота представляет собой бесцветную, сильно дымящую на воздухе жидкость. Она устойчива в водных растворах, в чистом виде взрывоопасна. [12]
Хлорная кислота, подвергшаяся частичному разложению, имеет цвет от темно-красного до коричневого. Чистая хлорная кислота в отличие от окислов хлора не обладает взрывчатыми свойствами. Частично разложившаяся хлорная кислота взрывает вследствие накопления в ней двуокиси хлора, обладающей сильными взрывчатыми свойствами. [13]
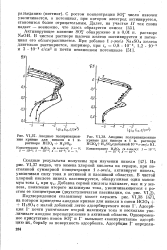 |
Анодные поляризационные кривые для никеля в 1 н. растворе НСЮ4 H2SO4.| Анодные поляризационные кривые для никеля в 1 н. растворе НСЮ4 Н2804сдобавкой 1Q - 6 г-экв / л KI. [14] |
Из рис. VI37 видно, что замена хлорной кислоты на серную, при постоянной суммарной концентрации 1 г-экв / л, активирует никель, увеличивая силу тока в активной и пассивной областях. В чистой хлорной кислоте никель пассивируется, обнаруживая один максимум тока in при фп. [15]
Страницы: 1 2