Концентрированная хлорная кислота
Cтраница 1
Концентрированная хлорная кислота действует и как водуотнимающее средство, чем пользуются для определения кремния, но не вольфрама. Впрочем, относительно последнего литературные данные противоречат друг другу. [1]
Концентрированная хлорная кислота является взрывоопасной. [2]
Концентрированная хлорная кислота ( 70 - 72 %) кипит без опасности взрыва. [3]
Концентрированная хлорная кислота ( 70 - 72 % - ная) кипит без опасности взрыва. [4]
Концентрированную хлорную кислоту и ее соли, перман-ганат калия, пероксиды металлов, а также другие окислители не разрешается хранить вместе с серой, фосфором, углем и другими восстановителями. [5]
Однако концентрированная хлорная кислота НС1О4 из-за искажения симметричной тетра-адрической формы иона СЮ4 действует как окислитель. Взрывоопасность безводной хлорной кислоты объясняется термической неустойчивостью существующего в ней гептаоксида дихлора С О. [6]
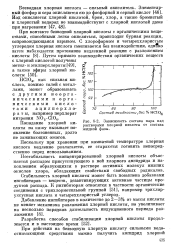 |
Зависимость состава пара над растворами хлорной кислоты от состава жидкой фазы. [7] |
Нестабильность концентрированной хлорной кислоты объясняется распадом присутствующего в ней хлорного ангидрида и накоплением образующихся в растворе активных молекул низших окислов хлора, обладающих свойствами свободных радикалов. [8]
Хранить концентрированную хлорную кислоту долго не разрешается, поскольку при комнатной температуре она разлагается, что может привести к самопроизвольным взрывам. [9]
При добавлении концентрированной хлорной кислоты к достаточно концентрированным растворам стеринов, содержащих 3 ( 3) - гидрокси - Д5 - ено-вую группу, в хлороформе обычно сразу же выпадает осадок хорошо кристаллизуемых, бесцветных солей хлорной кислоты. При нагревании эти соли легко загораются. [10]
После такой продувки концентрированная хлорная кислота в открытой посуде почти не дымит. [11]
Низкая растворимость в концентрированной хлорной кислоте и гораздо большая растворимость в кислотах с повышенной комплексообразующей способностью заставляет предполагать, что в растворах протактиния в большинстве кислот имеет место образование комплексов. [12]
Такая смесь известна как концентрированная хлорная кислота. [13]
Добавляют к остатку 5 мл концентрированной хлорной кислоты ( примечание 2), нагревают до разрушения пека, а затем добавляют 10 мл воды. Осторожно нагревают на горячей плите до полного растворения растворимого материала, охлаждают, переносят раствор в мерную колбу емкостью 500 мл ( примечание 3), добавляют 20 мл буферного раствора и доводят до метки водой. Приготавливают также холостой раствор, используя те же количества реагентов, без участия анализируемого материала. [14]
Миссан и Сухотин [4] исследовали взаимодействие концентрированной хлорной кислоты с продуктами ее разложения - окислами и низшими кислородными кислотами хлора. Снимая кривые катодной поляризации, они нашли потенциалы восстановления окислов хлора, растворенных в хлорной кислоте. Электрохимическое изучение окрашенной хлорной кислоты, уже подвергшейся разложению, показало, что продуктами ее распада помимо кислорода являются двуокись и трехокись хлора. Установлено также, что концентрированная хлорная кислота не подвергается восстановлению до тех пор, пока напряжение не станет равным 2 0 в. [15]
Страницы: 1 2 3 4