Кислородная кислота - фосфор
Cтраница 2
Если за основу взять эти формулы, то во всех кислородных кислотах фосфора, несмотря на его последовательно уменьшающуюся электро-валентность от 5 - J -, 4, 3 - f - до 1, фосфору должна быть приписана валентность в структурном значении этого слова, равная пяти. [16]
При гидролизе сернистых соединений азота образуются аммиак и кислородные кислоты серы, а при гидролизе сульфидов фосфора наряду с кислородными кислотами фосфора образуется сероводород. [17]
В присутствии влаги P4S3 при обычных температурах не изменяется, a P4S7 и Р45ю медленно разлагаются с выделением H2S и образованием кислородных кислот фосфора. [18]
В лаборатории, изучавшей кислородные кислоты фосфора, кончи лись запасы всех реактивов, кроме трихлорида и пентахлорида фосфо ра Тем не менее требовалось, не дожидаясь новых поставок, закончить начатую работу Тогда решили получить нужные кислоты из жидкого РС13 и кристаллического РС15 Сначала каждый из этих хлоридов сме шали с водой, а потом подвергли полученные растворы перегонке в ва кууме Какие кислородные кислоты фосфора удалось получить этим способом. [19]
Фосфор в окислительном состоянии 5 более устойчив, чем азот в том же состоянии; фосфорная кислота и фосфаты не являются эффективными окислителями. Кислородные кислоты фосфора имеют на один атом кислорода ( и на два атома водорода) больше, чем кислородные кислоты азота в соответствующих окислительных состояниях. [20]
Сернистые соединения азота при гидролизе выделяют аммиак и образуют кислородные кислоты серы. Напротив, при гидролизе сульфидов фосфора наряду с кислородными кислотами фосфора образуется сероводород. [21]
Одно из последних указаний [3] об умеренной нестабильности красного фосфора дает возможность предполагать значительную химическую активность со многими химическими агентами, в том числе и со щелочами. Так, например, при нормальной температуре и влажности красный фосфор медленно реагирует с парами воды и кислородом воздуха, образуя фосфин и смесь кислородных кислот фосфора. Этот процесс экзотермичен и ускоряется с повышением температуры. [22]
Расплавленный фосфор хорошо растворяет серу, но химическое взаимодействие наступает при достаточно высокой температуре. Указанные сульфиды могут быть перекристаллизованы в расплаве нафталина и выделены в виде желтых кристаллов. Водой все они медленно разлагаются с выделением сероводорода и образованием кислородных кислот фосфора. [23]
Расплавленный фосфор хорошо растворяет серу, но химическое взаимодействие наступает при достаточно высокой температуре. Из сульфидов фосфора лучше изучены Р48з, P4Sy и Р48ю - Указанные сульфиды могут быть перекристаллизованы в расплаве нафталина и выделены в виде желтых кристаллов. Водой все они медленно разлагаются с выделением сероводорода и образованием кислородных кислот фосфора. [24]
Сульфиды фосфора P4S3, P4S7 и P4S10 получают нагреванием серы при 100 с белым фосфором или при 250 с красным фосфором. Структура так называемого сульфида фосфора Р48ю аналогична структуре окиси Р4Ою ( рис. 130, стр. Сульфиды фосфора нерастворимы в воде, но легко гидролизуются, образуя H2S и кислородные кислоты фосфора. [25]
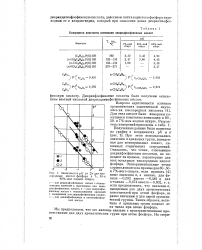 |
Кажущиеся константы ионизации диарилфосфиновных кислот.| Зависимость у К от 2 а для кислородных кислот фосфора в 7 -, 50-и 80 % - ном водном спирте. [26] |
Для этих кислот были измерены кажущиеся константы ионизации в 80 -, 50-и 7 % - ном водном спирте. При этом использовались значения а арильных групп, выведенные для моноарильных кислот, лишенных стерических затруднений. Оказалось, что точки, отвечающие диарилфосфиновым кислотам, не попадают на прямые, характерные для всех остальных кислородных кислот фосфора. Таким образом, величина а арильных групп зависит от их числа при атоме фосфора. [27]
Расплавленный фосфор хорошо растворяет серу, но химическое взаимодействие наступает при достаточно высокой температуре. Из сульфидов фосфора лучше изучены Р48з, P Sj и Р48ю - Указанные сульфиды могут быть перекристаллизованы в расплаве нафталина и выделены в виде желтых кристаллов. При нагревании сульфиды воспламеняются и сгорают с образованием РэОз и ЗОз-Водой все они медленно разлагаются с выделением сероводорода и образованием кислородных кислот фосфора. [28]
Характерным для сернистых соединений является очень значительное увеличение их устойчивости в направлении от азота к висмуту. Сернистые соединения азота при нагревании вспыхивают; сернистые соединения фосфора в отсутствие воздуха перегоняются без разложения, но на воздухе воспламеняются уже при умеренном нагревании. Значительно устойчивее сульфиды мышьяка, сурьмы и висмута, которые вследствие этого нередко встречаются в природе. Сурьма и висмут даже распространены в природе главным образом в виде сульфидов. Сернистые соединения азота при гидролизе выделяют аммиак и образуют кислородные кислоты серы. Напротив, при гидролизе сульфидов фосфоранаряду с кислородными кислотами фосфора образуется сероводород. Это показывает, что в сульфидах азота отрицательный заряд имеет азот, в сульфидах же фосфора, наоборот, сера. Как следует из способов образования, последнее справедливо также и для Сульфидов мышьяка, сурьмы и висмута, которые вследствие их крайней нерастворимости не разлагаются ни водой, ни разбавленными кислотами. [29]
Характерным для сернистых соединений является очень значительное увеличение их устойчивости в направлении от азота к висмуту. Сернистые соединения азота при нагревании вспыхивают; сернистые соединения фосфора в отсутствие воздуха перегоняются без разложения, но на воздухе воспламеняются уже при умеренном нагревании. Значительно устойчивее сульфиды мышьяка, сурьмы и висмута, которые вследствие этого нередко встречаются в природе. Сурьма и висмут даже распространены в природе главным образом в виде сульфидов. Сернистые соединения азота при гидролизе выделяют аммиак и образуют кислородные кислоты серы. Напротив, при гидролизе сульфидов фосфора наряду с кислородными кислотами фосфора образуется сероводород. Это показывает, что в сульфидах азота отрицательный заряд имеет азот, в сульфидах же фосфора, наоборот, сера. Как следует из способов образования, последнее справедливо также и для сульфидов мышьяка, сурьмы и висмута, которые вследствие их крайней нерастворимости не разлагаются ни водой, ни разбавленными кислотами. [30]
Страницы: 1 2 3