Сильная азотная кислота
Cтраница 1
Сильная азотная кислота также может вытеснять сульфогруппу. [1]
Образует азотный ангидрид N2O5 и сильную азотную кислоту HNO3, в которых проявляет высшую валентность по кислороду, равную пяти. С водородом азот также дает газообразное соединение NH3, в котором валентность азота равна трем. [2]
Образует азотный ангидрид N2O5 и сильную азотную кислоту HNOs, в которых проявляет высшую валентность по кислороду, равную пяти. С водородом азот также дает газообразное соединение NHs, в котором валентность азота равна трем. [3]
Здесь используется не только химическая энергия сильной азотной кислоты, но и анион ее, образующий ценную составную часть удобрения в виде нитрата кальция. Это обстоятельство является основным экономическим преимуществом азотнокислотной переработки фосфатов перед способами разложения их серной и соляной кислотами. В данном случае все ценные компоненты сырья ( фосфор, азот и калий) полностью переходят в состав удобрений, которые не содержат балластных примесей и имеют большое количество питательных веществ. Поэтому азотнокис-лотное разложение фосфатов является передовым технологическим процессом, основанным на комплексном использовании сырья. [4]
 |
Изменение свойств химических элементов в ряду литий. [5] |
Азот - типичный неметалл, газообразное вещество; в соединениях бывает положительно пятивалентным и отрицательно трехвалентным, образует довольно прочную сильную азотную кислоту. [6]
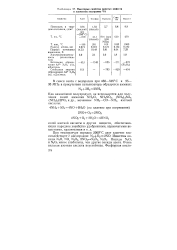 |
Некоторые свойства простых веществ и элементов подгруппы VA. [7] |
Оксиды N2O3 и N2O5 менее стабильны, чем другие оксиды азота. Очень сильная азотная кислота неустойчива. [8]
Все элементы VA-группы, за исключением висмута, образуют оксиды Э2Э5, имеющие кислотный характер. Им соответствуют сильная азотная кислота HNOs, слабые ортофосфорная и мышьяковая кислоты НзРС4 и HsAsO4 и малорастворимый в воде полигидрат Sb2Os иНаО, который переходит в раствор в виде гидро-ксокомплекса [ Sb ( H2O) ( OH) 5 ], обладающего слабокислотными свойствами. Оксиды 8263 существуют для всех элементов VA-группы. У гидроксидов висмута ( Ш) состава В1 ( ОН) з и BiO ( OH) преобладают основные свойства. [9]
Так, в растворителях более кислых, чем вода, степени диссоциации многих кислот уменьшаются. Например, в безводной уксусной кислоте сильная азотная кислота становится в 4000 раз слабее хлорной, хотя в воде эти кислоты близки по силе. Это зависит не только от уменьшения диэлектрической постоянной растворителя, но и от большой про-толитической функции уксусной кислоты. Сила же оснований в кислотных растворителях, наоборот, увеличивается. [10]
Ка-летка и Конечны [550] также использовали силикагель в качестве подложки, на которую наносили нерастворимые соединения гексацианоферратов никеля, меди, кадмия или цинка, способные действовать как катионообменники. Они могут удалять следовые количества ионов цезия даже из раствора сильной азотной кислоты. [11]
Имя самого видного из средневековых алхимиков осталось неизвестным; он подписывал свои труды именем Джабира, арабского алхимика, жившего за шесть веков до него. Этот Псевдо-Джабир был, вероятно, испанцем и жил в XIV в. Он также описал, как образуется сильная азотная кислота. [12]
Элемент азот, стоящий в естественной последовательности атомов за углеродом - уже явный неметалл, но среди неметаллов он один из самых неактивных. Заставить азот вступить во взаимодействие с кислородом исключительно трудно - для этого нужна температура гораздо выше 1000 градусов. Зато с водой окисел азота дает сильную азотную кислоту. [13]
Страницы: 1