Ниобиевая кислота
Cтраница 2
Исследование состава ниобиевой кислоты, осажденной из буферных растворов, Сообщ. [16]
Полиядерный характер частиц ниобиевой кислоты сохраняется даже при сильном разбавлении, Хэрди и Скаржилл [71 ] обнаружили, что в азотнокислом растворе 95Nb даже при концентрации ниобия 10 - 7 М и концентрации кислоты ниже 2 М присутствуют в большом количестве полимерные частицы. [17]
При составлении электролита ниобиевую кислоту разбавляют во фт РистовоДородной кислоте, после чего вводят остальные компоненты. Электролит требует предварительной проработки в течение 2 ч, С повышением температуры и плотности тока покрытия меняют свой цвет от блестящих светло-серых до блестящих темно-серых. [18]
Растворы гидроокиси ниобия ( ниобиевой кислоты) в концентрированной ( - 75 % - ной) серной кислоте могут быть восстановлены электролитически. Образующийся сульфатный комплекс с эмпирической формулой HNb3 ( SO4) e - x H2O выделяется в виде игольчатых красно-коричневых кристаллов. Растворы танталовой кислоты в серной кислоте в этих условиях восстанавливаются гораздо труднее. Средняя формальная валентность ниобия в комплексе равна 3.67; это означает, что на два трехвалентных атома ниобия приходится один пятивалентный. Соли этого комплекса, содержащие катионы щелочных металлов или аммония с эмпирической формулой K8Nbe ( OH) 6 ( SO4) 12 - 18H2O [ или K8NbeO3 ( SO4) 12 - 21H2O ] более устойчивы, чем исходный кислый комплекс. Такие соли могут быть получены в виде кристаллических продуктов при добавлении сернокислых растворов сульфатов щелочных металлов или аммония к восстановленному раствору комплекса в серной кислоте. Бора на 1 атом ниобия), а четыре - диамагнитны. [19]
При добавлении аммиака щавелевокислый раствор ниобиевой кислоты становится нестойким и при рН 5-т-б, когда большая часть щавелевой кислоты полностью ионизирована ( ионы С2О42 -), из него начинает осаждаться ниобиевая кислота. Напротив, упомянутые выше комплексы с другими а-оксикарбоновыми кислотами при добавлении аммиака не разлагаются. Так, если комплексообра-зователями являются более слабые кислоты, например гликолевая и молочная, то при добавлении аммиака ( для поддержания рН 8 - ь9) скорость растворения ниобиевой кислоты резко возрастает. Шеллер [131] сообщил также, что растворы ниобиевой или танталовой кислоты в виннокислом аммонии более устойчивы, чем их растворы в винной кислоте. Следовательно, можно сделать вывод, что, по-видимому, в каждом случае комплексообразователем является анион кислоты. [20]
Часто радиоактивный Nb выделяют осаждением ниобиевой кислоты из щавелевокислых растворов с последующей радиохимической очисткой экстракцией ТБФ, диизопропилкетоном, купфероном в СНС13 и другими растворителями. [21]
Выпавший при этом белый осадок ниобиевой кислоты полностью растворяется. После охлаждения раствора приливают 2 мл 10 % раствора винной кислоты, переливают все в мерную колбу емкостью 100 мл, доливают водой до метки и перемешивают. При содержании ниобия от 0 4 до 5 % отбирают 10 мл ( при содержании ниобия более 5 % - 1 - 2 мл) полученного раствора в мерную колбу емкостью 100 мл, приливают 10 мл 0 05 % раствора арсеназо I, 25 мл НС1 и нагревают до кипения. После охлаждения доливают до метки водой и перемешивают. Приготовленный раствор оставляют стоять на сутки, после чего измеряют его оптическую плотность по отношению к нулевому раствору, для приготовления которого используют те же реактивы. Неизвестную концентрацию ниобия находят по калибровочной кривой, построенной по стандартным растворам ниобия с добавлением соответствующих количеств чистого титана. Стандартные окрашенные растворы ниобия приготавливают так же, как и исследуемый раствор. [22]
Как следует из сказанного, ниобиевую кислоту получают теми же методами, которые используются для получения кремневой ( стр. Химические свойства ее сходны со свойствами оловянной кислоты. Студенистый осадок ниобиевой кислоты обладает очень слабыми основными свойствами. Содержание воды в нем высокое и переменное, при нагревании оно необратимо снижается. Ниобиевая кислота образует коллоидные растворы в тех же условиях, что и кремневая и оловянная кислоты. По этой причине этому соединению приписывают скорее формулу гидратированной окиси ниобия Nb2O5 - лгНоО, чем какой-либо определенной ниобиевой кислоты. [23]
Перекись водорода дает желтую окраску с ниобиевой кислотой, растворенной в концентрированной серной или в смеси концентрированных серной и фосфорной кислот; максимум поглощения наблюдается при 365 нм. [24]
Эдмистер и Албриттон [134], упаривая раствор свежеосажденной ниобиевой кислоты в виной кислоте, получили кристаллическое соединение ( С4Н4О6) 2 NbOH, в котором с каждым атомом ниобия связаны две молекулы винной кислоты. Авторы приписали ему структурную формулу, из которой видно, что четыре атома водорода кислоты остаются в комплексе, образующемся за счет конденсации гидроксильных групп винной кислоты с ниобиевой кислотой. [25]
Розе описывает образование ярко-синей окраски в кислом растворе ниобиевой кислоты в присутствии цинковой пластинки, ссылаясь при этом на подобные опыты Велера и Густава Розе. [26]
При наличии в растворе мути - частичное выпадение ниобиевой кислоты - анализ считают испорченным. [27]
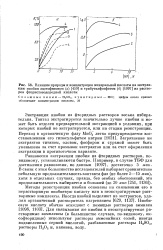 |
Влияние природы и концентрации минеральной кислоты на экстракцию ниобия ацетофеноном ( а и трибутилфосфатом ( б из растворов фтористоводородной кислоты. [28] |
Методы реэкстракции ниобия основаны на связывании его в нерастворимую ниобиевую кислоту или в неэкстрагируемые растворимые комплексы. Для связывания же ниобия в неэкстрагируемые растворимые комплексы ( в большинстве случаев, по-видимому, ок-софторидные) используют растворы аммонийных солей, иногда подкисленные серной кислотой, разбавленные растворы H2S04, растворы Н202 и, наконец, воду. [29]
Радиохимическая очистка проводится путем осаждения фторцирконата Ва и переосаждения ниобиевой кислоты. Метод применим при определении Nb в продуктах деления и в сточных водах. [30]
Страницы: 1 2 3 4