Окисляющая кислота
Cтраница 2
Эти соли получаются растворением металлического железа в окисляющих кислотах, взаимодействием тригидроксида с кислотами или окислением солей железа ( II) азотной кислотой. Это вещество светло-коричневого цвета, хорошо растворимо в поде и легко гидролизуется. [16]
Элементы, труднее окисляемые, растворяются при действии окисляющих кислот ( например, азотной кислоты): серебро, мышьяк, висмут, бор ( нагревают с обратным холодильником), кадмий, медь, галлий, германий, индий, марганец, ртуть, молибден, никель, свинец, селен, теллур, таллий, ванадий. [17]
Элементы, труднее окисляемые, растворяются при действии окисляющих кислот ( например, азотной кислоты): серебро, мышьяк, висмут, бор ( нагревают с обратным холодильником), кадмий, медь, галлий, германий, индий, марганец, ртуть, молибден, никель, свинец, селен, теллур, таллий, ванадий. [18]
Гораздо более сильное разрушительное действие на полимерные материалы оказывают окисляющие кислоты, большее чем неокисляющие и несколько более сильное, чем окислители некислотного характера. [19]
Сцепление с металлическим слоем значительно повышается после травления поверхности окисляющими кислотами или обработки тонким абразивом. [20]
Марганец весьма электроположителен и легко растворяется в разбавленных не окисляющих кислотах. [21]
Получают соли железа ( III) растворением металлического железа в окисляющих кислотах или взаимодействием гидроксида железа ( III) с кислотами. Это соединение бурого цвета, хорошо растворимо в воде и легко гидролизу ется. [22]
Характеристики: Эти материалы устойчивы к химическому воздействию, за исключением сильных окисляющих кислот и определенных органических растворителей. Они легкие, имеют высокую степень ударной вязкости, низкую водопоглощаемость, а также являются недорогими. [23]
Промышленность начала выпускать замазку арзамит 7 на основе совмещенной фенолоформальдегидной смолы, стойкой в окисляющих кислотах сильной степени агрессивности. [24]
Так, Аи, Pt, Ag стойки к коррозии во всех средах, кроме некоторых концентрированных окисляющих кислот, а Си, Sn, Pb - во влажной атмосфере, морской воде и многих органических кислотах. [25]
Наиболее пассивированной поверхностью обладает хром, который при обычных температурах не взаимодействует с водой и с окисляющими кислотами ( HNO3; HNO3 HC1), но реагирует с соляной и с разбавленной серной кислотами. [26]
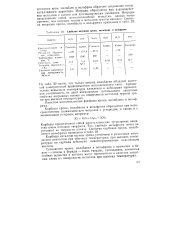 |
Свойства нитридов хрома, молибдена и вольфрама. [27] |
Карбиды металлов группы хрома устойчивы к различным химическим реагентам при обычных температурах; при высоких температурах на карбиды действуют концентрированные окисляющие кислоты. [28]
Платиновые металлы, поскольку их электродные потенциалы лежат в положительной области ряда напряжений, могут реагировать только лишь с окисляющими кислотами. [29]
При разложении металлов и сплавов, содержащих фосфор в виде фосфидов, для предотвращения образования летучего фосфористого водорода применяют лишь окисляющие кислоты, смесь азотной и соленой кислот, или разлагают сплавлением с перекисью натрия. Часть фосфора после разложения в кислотах находится в трехвалентном состоянии; для окисления его до ортофосфорной кислоты обычно применяют мар-ганцевокислый калий. [30]
Страницы: 1 2 3 4