Фтористоводородная кислота
Cтраница 2
Фтористоводородная кислота обычно бывает загрязнена следами меди, свинца и цинка. Для очистки от этих примесей кислоту подвергают не менее чем трехкратной перегонке в специальном перегонном аппарате, изготовляемом из платины или палладия. [16]
Фтористоводородная кислота более или менее энергично реагирует с большинством металлов. Однако во многих случ-аях реакция протекает лишь на поверхности металла, после чего последний оказывается защищенным от дальнейшего действия кислоты слоем образовавшейся труднорастворимой соли. Так ведет себя, в частности, свинец, что и позволяет пользоваться им для изготовления частей устойчивой к действию HF аппаратуры. [17]
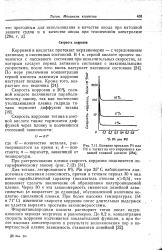 |
Влияние присадок Pt или Pd к титану на его коррозию в кипящей соляной кислоте [ 28а ]. [18] |
Фтористоводородная кислота растворяет титан после индукционного периода энергично и равномерно. [19]
 |
Диффузия радиоактивного фторида при комнатной температуре в присутствии силикона и в его отсутствие.| Насадка прибора для отделения фторида микродиффузией. [20] |
Фтористоводородная кислота поглощается импрегнированной бумагой, закрепленной в полимерной крышке полиэтиленовой банки вместимостью 20 мл. [21]
Фтористоводородная кислота отличается от НС1, НВг и HI тем, что она в газообразном состоянии образует сложные молекулы, и дает кислые соли, содержащие ионы F - Н - F ( см. раздел, посвященный водородной связи, стр. Структура молекулы H S в газовой фазе была определена с помощью метода дифракции электронов ( стр. Хп, которые будут описаны при изложении химии соответствующих элементов. [22]
Фтористоводородная кислота, 35 - 45 % - ный раствор фтористого водорода в воде - прозрачная бесцветная жидкость, дымящая на воздухе. Легко разъедает стекло и другие вещества, содержащие кремний, поэтому ее хранят в сосудах из парафина, поливинилхлорида, бакелита или полиэтилена. Применяется в синтезе для получения неорганических солей и органических фтор-производных и в анализе для разложения силикатов и удаления кремневой кислоты. Большое значение имеет фтористоводородная кислота особой чистоты как один из основных химических продуктов для полупроводниковой техники. [23]
Фтористоводородная кислота взаимодействует с большинством металлов, но не реагирует с золотом и платиной. Соли ее, называемые фторидами, труднорастворимы в воде, но фтористое серебро AgF в отличие от других галидов серебра хорошо растворяется в воде. [24]
 |
Фтористоводородная горелка. [25] |
Фтористоводородная кислота ( в незначительных количествах) обладает свойством усиливать дрожжевое брожение, может служить дезинфицирующим средством. [26]
Фтористоводородная кислота представляет собой раствор HF в воде. В противоположность другим галоидоводо-родным кислотам она является кислотой средней силы. Большинство ее солей - фторидов - малорастворимо в воде. Исключение составляют фториды щелочных металлов ( кроме Li), а также AgF, HgF2, SnF4, FeFs и AlFa. Все соли HF ядовиты. Сама она при попадании на кожу вызывает образование болезненных и труднозаживаемых ожогов, особенно под ногтями. [27]
Фтористоводородная кислота представляет собой раствор HF в воде. В противоположность другим галоидоводородным кислотам она является кислотой средней силы. Большинство ее солей - фторидов - мало растворимо в воде. Все соли HF ядовиты. Сама она при попадании на кожу вызывает образование болезненных и трудно заживаемых ожогов, особенно под ногтями. [28]
Фтористоводородная кислота представляет собой раствор HF в воде. В противоположность другим галоидоводородным кислотам она является кислотой средней силы. Большинство ее солей - фторидов - мало растворимо в воде. Исключение составляют фториды щелочных металлов ( кроме Li), а также AgF, Hgp2, SnF4, FeFa и AlFs. Все соли HF ядовиты. Сама она при попадании на кожу вызывает образование болезненных и трудно заживаемых ожогов, особенно под ногтями. [29]
Фтористоводородная кислота стала чрезвычайно необходима для мировой химической индустрии. Она является основным сырьем для производства неорганических фторидов и фторугле-родов, катализатором для ряда органических реакций, например алкилирования, реагентом для травления металлов, стекла и важнейшим сырьем для получения фтора. Опубликованы два исчерпывающих обзора27 - 29 о производстве и применении HF и других фторсодержащих продуктов. [30]
Страницы: 1 2 3 4