Образовавшаяся муравьиная кислота
Cтраница 2
Для определения метилольных групп в фенолоформальдегид-ных резольных смолах используют щелочное иодирование фено-лоформальдегидного полимера с последующим подкислением раствора избытком НС1 и потенциометрическим титрованием смеси хлористоводородной, иодистоводородной и муравьиной кислот. В этом случае количество образовавшейся муравьиной кислоты эквивалентно содержанию метилольных групп в образце. [16]
Смесь взбалтывают 2 ч с избытком периодата калия. После фильтрования реакционной смеси образовавшуюся муравьиную кислоту титруют щелочью в присутствии метилового красного и вычисляют содержание глицерина. [17]
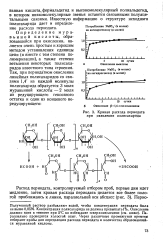 |
Кривая расхода периодата при окислении полисахарида. [18] |
Параллельно проводится холостой опыт. Через различные промежутки времени отбирают пробы для определения расхода периодата и количества образовавшейся муравьиной кислоты. [19]
В соответствии с этим для установления строения олигосахаридов используют количественное определение расхода периодата и образовавшейся муравьиной кислоты и формальдегида, а также изучение природы моноса-харидгых ЗЕеньев, оставшихся неизмснрыки при действии окислителя. Примером использования периодатного окисления может служить установление строения восстанавливающего трисахарида XVI, построенного из остатков D-ксилозы. На основании данных о скорости его гидролиза было установлено отсутствие фуранозидных связей. Трисахарид поглощал 4 моль периодата с образованием 3 моль муравьиной кислоты; при гидролизе продукта окисления была получена D-ксилоза. Неокисляемый остаток ксилозы может занимать одно из двух положений: а) среднее звено с 1 - 3-связью в неразветвленном трисахариде; б) восстанавливающее звено с 1 - 2 - и 1 - - 4-связями в разветвленном трисахариде. Однако последняя структура должна была бы привести к поглощению 4 моль периодата с образованием 2 моль мурагьиной кислоты, что не согласуется с экспериментальными данными. Таким образом, исследуемый три-сахарид имеет неразветвленную структуру, а концевой осттгок присоединен к среднему звену 1 - - 3-связью. Концевой остаток ксилопиранозы должен поглощать 2 моль периодата и давать 1 холь муравьиной кислоты, следовательно, на окисление восстанавливающего звена расходуется 2 моль периодата и выделяется 2 моль муравьиной кислоты. Образование второго моля муравьиной кислоты связано с отщеплением формильного остатка, происходящего из гликозид-ного атома углерода. Таким образом, строение трисахарида установлено полностью, кроме конфигурации гликозид-ных связей. [20]
Ниже приведены общие методы [1, 5] окисления полисахаридов. Обычно полисахарид окисляют разбавленным раствором периодата натрия на холоду, измеряя через определенные промежутки времени количества образовавшейся муравьиной кислоты и израсходованного периодата. Муравьиную кислоту определяют прямым титрованием стандартным раствором щелочи [11 -13], или косвенно - по количеству иода, выделившегося из раствора иодида и иодата калия [12, 14], или по выделению углекислого газа ( определяемого манометрически [15]) из бикарбонатного буферного раствора. [21]
В результате окисления возникают две альдегидные группы, а при наличии третьего свободного гидроксила и дальнейшего окисления образуется муравьиная кислота, которую можно оттитровать. Три подряд свободные окисляющиеся гидроксилыше группы содержатся у гексозанов только в конце цепи; отсюда, определив количество образовавшейся муравьиной кислоты, устанавливают величину молекулы полисахарида, а по количеству пошедшей на окисление йодной кислоты - и способ связи. [22]
Что касается экспериментального обоснования этой теории, то оно поражает своей скудостью. В ряде опытов Вислиценус определял количество кислорода, которое выделяется из смеси перекиси водорода и двууглекислых щелочей при разных условиях, но точного количественного определения образовавшейся муравьиной кислоты он не производил. По его собственным словам, муравьиной кислоты было настолько мало, что точное количественное определение представлялось невозможным. [23]
Если в анализируемой смеси присутствует глицерин, при анализе последнего в результаты определения вносится поправка на муравьиную кислоту, образующуюся при окислении вторичной гидрокснльной группы. Вторые SO мл аликвота окисляют раствором перйодата, как указано выше, затем избыток йодной кислоты удаляют, добавив 1 мл чистого гликоля, и титруют образовавшуюся муравьиную кислоту в присутствии индикатора метилового красного. [24]
В пробирку наливают 1 мл молочной кислоты и 1 мл концентрированной серной кислоты. Закрыв пробирку пробкой с газоотводной трубкой, нагревают смесь до кипения. При разложении образовавшейся муравьиной кислоты выделяется оксид углерода, который поджигают. [25]
К охлажденному до 5 С раствору 34 2 г ( 0 16 моль) метапериодата натрия в 400 мл воды добавляют 15 5 г ( 0 08 моль) метил-р-о-глюко - пиранозида. Дозировку проводят порциями в течение 5 мин при постоянном перемешивании. Реакционной смеси дают нагреться до - 25 С и образовавшуюся муравьиную кислоту нейтрализуют бикарбонатом натрия ( 6 1 г, 0 9 экв. Фильтрат упаривают в вакууме и полукристаллическую массу смешивают с 200 мл спирта. Отфильтровав нерастворимые продукты, растворитель отгоняют в вакууме и сиропообразный остаток растворяют в 100 мл воды. Щелочь приливают постепенно в течение 5 мин, поддерживая температуру реакционной массы О С. Перемешивание продолжают еще 10 мин и раствор отделяют декантацией. Колонку промывают водой и элюаты упаривают в вакууме до сиропообразного состояния. Остаток высушивают упариванием с двумя порциями спирта и двумя порциями этилацетата. [26]
Муравьиную кислоту, количество которой эквивалентно количеству глицерина, определяют титрованием стандартным раствором щелочи. Образовавшийся при окислении пропиленгликоля ацеталь-дегид отделяют от формальдегида и определяют бисульфитным методом. Количество этиленгликоля находят по разности, определив количество периодата, израсходованное на окисление суммы всех трех спиртов, или общее количество образовавшихся альдегидов. Концентрацию каждого из трех спиртов можно найти также, определяя количества образовавшейся муравьиной кислоты, формальдегида ( в присутствии ацетальдегида цианидным методом) и общее количество альдегидов. [27]
Муравьиную кислоту, количество которой эквивалентно количеству глицерина, определяют титрованием стандартным раствором щелочи. Образовавшийся при окислении пропил енгликоля ацеталь-дегид отделяют от формальдегида и определяют бисулъфитным методом. Количество этиленгликоля находят по разности, определив количество периодата, израсходованное на окисление суммы всех трех спиртов, или общее количество образовавшихся альдегидов. Концентрацию каждого из трех спиртов можно найти также, определяя количества образовавшейся муравьиной кислоты, формальдегида ( в присутствии ацетальдегида цианидным методом) и общее количество альдегидов. [28]
Используя С11 с периодом полураспада 20 5 мин. Аллеи и Рубен [ А5 ] смогли проследить за атомами углерода в карбоксильных группах фумаровой кислоты НООС-СНСН-СООН при окислении ее перманганатом при 40 С. Следовало решить вопрос, образуется ли муравьиная кислота за счет углеродов метенильной группы или карбоксильной или же за счет атомов углерода обеих этих групп. Полученный в обоих случаях карбонат кальция отфильтровывали, промывали, сушили и взвешивали. Было показано, что образовавшаяся муравьиная кислота неактивна; следовательно, она образуется только из углеродных атомов метенильных групп фумаровой кислоты. [29]
Страницы: 1 2