Технециевая кислота
Cтраница 2
Технетат ( ы) 299, 307, 309; II - 313 Технециевая кислота 298 ел. [16]
Термодинамическая вероятность 188 Термохимия 173 Терм спектральный 13, 14, 34 Тетраванадиевая кислота 501 Тетрафтороборная кислота 348 Тетрафтороиодная кислота 471 Тетрахлорозолотая кислота 557 Тетрахроматы 516, 521 Тетрацианоплатиновая кислота 547 Технециевая кислота 521, 525 Технеций 50, 521 - 529 Тиокарбамид ( тиомочевина) 393 Тиокарбонаты 371 Тионилгалогениды 445, 449 Тиосерная кислота 441 Тиостаннаты 390 Тиоугольная кислота 371, 393 Тиохроматы 513 Тиоцианаты 373, 393 Титан 50, 486 - 497 Титанаты 493 Титанила соединения 494 Титановые кислоты 493 Торий 50, 573 - 576 Трисилиламин 377 Тритий 454 ел. [17]
Термодинамическая вероятность 188 Термохимия 173 Терм спектральный 13, 14, 34 Тетраванадиевая кислота 501 Тетрафтороборная кислота 348 Тетрафтороиодная кислота 471 Тетрахлорозолотая кислота 557 Тетрахроматы 516, 521 Тетрацианоплатиновая кислота 547 Технециевая кислота 521, 525 Технеций 50, 521 - 529 Тиокарбамид ( тиомочевина) 393 Тиокарбонаты 371 Тионилгалогениды 445, 449 Тиосерная кислота 441 Тиостаннаты 390 Тиоугольная кислота 371, 393 Тиохромвты 513 Тиоцианаты 373, 393 Титан 50, 486 - 497 Титанаты 493 Титанила соединения 494 Титановые кислоты 493 Торий 50, 573 - 576 Трисилиламин 377 Тритий 454 ел. [18]
Известные соединения технеция имеют большое сходство с соединениями рения. Технециевая кислота НТс04 восстанавливается сравнительно легко. [19]
Теплоты образования семиокиси технеция и технециевой кислоты, потенциал пары технеций ( 4) - технеций ( 7) и диаграмма потенциалов технеция. [20]
Способность технеция эффективно экстрагироваться различными органическими соединениями использована во многих методах его отделения. Технеций извлекается органическими растворителями как в виде технециевой кислоты или ее солей, так и в виде различных комплексных соединений, в которых технеций находится в низших валентных состояниях. По характеру извлечения такие ионные ассоциаты можно подразделить на группы: 1 - ассоциаты, содержащие большой органический катион или основание; 2 - ассоциаты, содержащие неорганические катионы. [21]
При нагревании с кислородом металлический технеций горит с образованием окиси технеция ( МН) ТсгО7 желтого цвета. При растворении в воде она переходит в технециевую кислоту НТсО4, которая после упаривания раствора остается в виде кристаллов красного цвета. Восстановлением этого соединения водородом при 1000 или восстановлением пертехнетата аммония при 500 получают металлический технеций. Полярографическим методом установлено, что технеций в соединениях может быть четырех -, шести - и семивалентным. [22]
Светло-желтый, летучий, при нагревании разлагается. Проявляет кислотные свойства, реагирует с водой, образует сильную технециевую кислоту НТсО4; концентрированный раствор - темно-красный, разбавленный раствор - бесцветный. Реагирует со щелочами, гидратом аммиака. [23]
Ядра образовавшихся в результате деления изотопов 106Тс и 108Тс имеют форму, промежуточную между сферической и деформированной; поэтому, как и для изотопов церия, интересно иметь данные о распаде этих изотопов. И в этом методе галогены удаляли с помощью AgCl, после чего технеций в виде анионов технециевой кислоты извлекали с помощью хлороформеяиого раствора хлорида тетрафенилареония, нанесенного на гранулированную пластмассу; вместе с технецием частично извлекались благородные газы. Технеций элюировали 2 М раствором HNO3, содержащим пер-ренат, который служил носителем для последующего соосажде-ния технеция с использованием водного раствора хлорида тетрафениларсония. [24]
Технеций - тяжелый металл плотностью 11 50, кристаллизуется в ге-ксагональ ной плотной упаковке и плавится при 2127 С. По химическим свойствам он больше похож на рений, чем на марганец. Последний при растворении в воде образует сильную одноосновную технециевую кислоту. Известны соли типа МеТсО, которые по своей окислительной активности занимают промежуточное положение между перманганатами и перренатами. [25]
 |
Влияние природы и концентрации. [26] |
На адсорбцию технеция большое влияние оказывает не только природа постороннего аниона, но и кислотность раствора. Как видно из рис. 6, поглощение технеция значительно больше из нейтральных солей, чем из кислот с таким же анионом. Вероятно, это явление обусловлено образованием в довольно кислых средах малодиссоциированной технециевой кислоты, которая не поглощается анионитом. Кроме того, причиной различия может служить различие в коэффициентах активностей в фазе смолы. Влияние концентрации постороннего аниона проявляется по-разному. Такое поведение становится понятным в связи с описанными выше спектрофотометрическими исследованиями. Наблюдаемый ход кривой является следствием появления конкурирующего с процессом вытеснения процесса поглощения технеция смолой вследствие образования анионного хлоридного комплекса технеция более низкой валентности. [27]
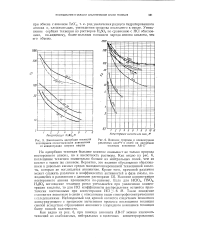 |
Зависимость адсорбции технеция.| Влияние природы и концентрации. [28] |
На адсорбцию технеция большое влияние оказывает не только природа постороннего аниона, но и кислотность раствора. Как видно из рис. 6, поглощение технеция значительно больше из нейтральных солей, чем из кислот с таким же анионом. Вероятно, это явление обусловлено образованием в довольно кислых средах малодиссоциированной технециевой кислоты, которая не поглощается анионитом. Влияние концентрации постороннего аниона проявляется по-разному. Такое поведение становится понятным в связи с описанными выше спектрофотометрическими исследованиями. Наблюдаемый ход кривой является следствием появления конкурирующего с процессом вытеснения процесса поглощения технеция смолой вследствие образования анионного хлоридного комплекса технеция более низкой валентности. [29]
Окислы и гидраты окислов. Семиокись получается в виде желтых кристаллов при горении элементарного технеция в кислороде. Соли технециевой кислоты - - пертехнаты - растворимы лучше, чем соответствующие перренаты, которым они изоморфны. Пертехнаты соосаждаются с перренатами, перхлоратами и другими аналогичными ионами. [30]
Страницы: 1 2