Фтороводородная кислота
Cтраница 2
Разложение фтороводородной кислотой непригодно, если пробы содержат диоксид олова или пириты. Растворение металлов и сплавов во фтороводородной кислоте с выделением водорода описано в разд. [16]
Разложение фтороводородной кислотой широко используется при анализе многих природных и искусственных силикатов, а также других материалов, в частности оксидов ниобия, тантала, титана и циркония, ниобиевых и танталовых руд и руд с низким содержанием кремневых включений. Разложение устойчивых силикатов рекомендуется проводить в автоклавах. [17]
Структуры гидратов фтороводородной кислоты HF не расшифрованы. Температуры плавления гидратов соляной кислоты с повышением степени гидратации последовательно понижаются: - 15 4, - 17 4 и - 29 4 СС; все три структуры известны. Кратчайшее расстояние между атомами кислорода и хлора соседних слоев 3 43 А. [18]
А Одну фтороводородную кислоту редко используют для разложения анализируемых материалов. А При разложении только фтороводородной кислотой к пробе добавляют, как правило, ее в большом избытке ( 25 - 50 мл 40 % - ного раствора HF на 1 г пробы) и оставляют смесь на несколько часов, лучше на ночь. Растворение ускоряется нагреванием реакционной смеси до 80 С при периодическом перемешивании. Тольки немногие вещества не разрушаются в таких условиях. [19]
При ожогах фтороводородной кислотой пользуются 2 % - ным раствором СаС12 или 20 % - ной суспензией оксида магния в глицерине. [20]
Реагирует с концентрированной фтороводородной кислотой, разлагается щелочами. [21]
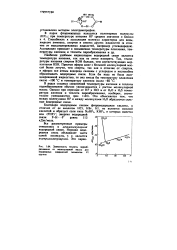 |
Зависимость теплоты парообразования от молекулярной массы для водородных соединений элементов VI группы. [22] |
Благодаря водородным связям фтороводородная кислота, в отличие от ее аналогов HCI, НВг, HI, не является сильной кислотой и образует соли типа NaHFj, KHFj, в которых имеется ион ( FHF); энергия водородной связи F-H - - - F равна 113 кДж / моль. [23]
По этой причине фтороводородная кислота разъедает стекло и стеклянной аппаратурой нельзя пользоваться при работе с HF или FJ. Фтор не взаимодействует с совершенно сухим стеклом, но так как он реагирует с водой с образованием HF, стеклянные изделия разрушаются. [24]
Раствор HF ( фтороводородная кислота) является кислотой средней силы. [25]
 |
Зависимость теплоты парообразования от молекулярной массы для водородных соединений элементов VI группы. [26] |
Благодаря водородным связям фтороводородная кислота, в отличие от ее аналогов HCI, HBr, HI, не является сильной кислотой и образует соли типа NaHF2, KHF2, в которых имеется ион ( FHF); энергия водородной связи F-H - F равна ИЗ кДж / моль. [27]
Если через раствор фтороводородной кислоты пропустить 96484 Кл электричества, то будет перенесено 2 моль ионов фтора. [28]
Если через раствор фтороводородной кислоты пропустить 96 484 Кл электричества, то будет перенесено 2 моль ионов фтора. [29]
Другим способом получения фтороводородной кислоты из флюорита является пирогидролиз при температуре выше 1200 С. [30]
Страницы: 1 2 3 4