Альдолаз
Cтраница 1
Альдолаз а-расщепляет гексозодифосфат на две фосфотриозы: диоксиацетонфосфат и глицеринальдегидфосфат. Она широко распространена в тканях животных и растений, а также в микроорганизмах. Количество ее в скелетных мышцах кролика достигает почти 5 % от всего растворимого в воде белка. Выделенный из мышц Барановским миоген А оказался альдолазой. Альдолазная активность миогена мышц установлена Энгельгардтом. Мышечная и дрожжевая альдолазы, называемые также зимогексазой, отличаются одна от другой только в средствах инактивации. [1]
Альдолаза встречается в различных органах и тканях человека и животных. Содержание ее в сыворотке крови здоровых людей незначительно, а при болезни Боткина резко повышается за счет выхода этого фермента в кровь из клеток печени. [2]
Альдолаза содержит свободные SH-группы; некоторые из них играют важную роль в каталитической активности, но основная их функция состоит в поддержании нативной структуры. В состав активного центра входят две е-аминогруппы остатков лизина. Их функция заключается в осуществлении связи фермента с одним из субстратов ( диоксиацетонфосфатом) путем образования промежуточного соединения типа основания Шиффа. [3]
Альдолаза относится к классу альдегид-лиаз. Реакция расщепления - сопровождается образованием двойной связи. [4]
Альдолаза катализирует реакцию расщепления фруктозо-1 6-ди-фосфата на 3-фосфоглицериновый альдегид и фосфодиоксиацетон. [5]
Альдолаза играет важную роль в процессах обмена веществ. [6]
Активность альдолазы из Aspergillus niger, участвующей в образовании лимонной кислоты, подавляется 2 2 - ДП. [7]
Выделение альдолазы из скелетных мышц кролика и изучение ее свойств в растворимом и иммобилизованном состоянии. [8]
Активность альдолазы может быть измерена двумя методами: химическим, основанным на определении концентрации продуктов реакции - фосфотриоз ( по нарастанию щелочнолабильного фосфоря), и энзиматическим, в сопряженной системе, содержащей помимо альдолазы и фруктозо-1 6-дифосфата также НАД и глицеральдегид-3 - фосфат-дегидрогеназу или НАДН и глицерол-3 - фосфатдегидрогеназу. Скорость альдолазнои реакции определяют по нарастанию или убыли НАДН. [9]
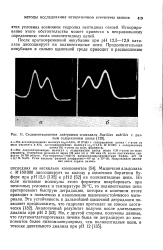 |
Седиментационные диаграммы а-амилазы Bacillus subtilis с разным содержанием цинка. [10] |
Мышечная альдолаза с Ml60000 диссоциирует на холоду в щелочном боратном буфере при-р Н 12 5 [132] и рН2 [52] на полипептидные цепи. Но если нативные молекулы этого фермента инкубировать при щелочных условиях и температуре 20 С, то полипептидные цепи претерпевают быструю деградацию, которая в конечном итоге приводит к появлению и накоплению щелочноустойчивого материала. [11]
В альдолазах имеются свободные SH-группы, из которых некоторые необходимы для проявления каталитической активности. [12]
Эти формы альдолазы имеют различную локализацию. [13]
Происходит активация альдолаз и аминофераз сыворотки, изменяется активность моноаминооксидазы, нарушается белковый и аминокислотный обмен. [14]
Наконец, альдолаза, как об этом упоминалось выше, катализирует дей-териевый или тритиевый обмен только между одним из атомов водорода диоксиацетонфосфата и растворителем. [15]
Страницы: 1 2 3 4