Колицин
Cтраница 1
Колицин растворим в воде при любых значениях рН, но нерастворим в обычных органических растворителях за исключением уксусной кислоты и пиридина. Не имеет температуры плавления. Легко диффундирует через целлофан. Устойчив как в сухом виде, так и в водных растворах. [1]
Молекулы колицина присоединяются к специальным рецепторам - молекулам липополисахаридам, выступающим из внешней жесткой оболочки бактерии. Присоединив молекулу колицина К ( или Е1), бактерия некоторое время продолжает функционировать нормально. [2]
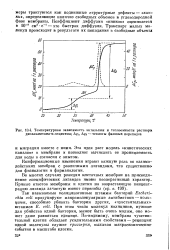 |
Температурная зависимость энтальпии и теплоемкости раствора, дипальмитоил-сс-лецитина. Д. 1, Д. 2 - теплоты фазовых переходов. [3] |
При этом число молекул колицинов, нужное: для убийства одной бактерии, может быть очень малым, оно может даже равняться единице. По-видимому, мембрана чувствительной клетки обладает усилительными свойствами - рецепцияс одной молекулы служит триггером, вызывая макроскопические-события в масштабе клетки. [4]
Для объяснения наблюдаемых эффектов влияния молекул колицина на нормальные и мутантные бактерии E-coli делается предположение, что внедрение молекулы колицина в клетку сопровождается снижением мембранной разности потенциалов. Снижение разности потенциалов приводит к прекращению активного транспорта лактозы, глютамина, ионов калия и магния через мембрану. В нормальной бактериальной клетке фермент АТФ-аза, находящийся в мембране в безнадежной попытке восстановить необходимую разность потенциалов, производит интенсивный гидролиз молекул АТФ, снижая количество этих молекул внутри клетки. Следствием уменьшения числа молекул АТФ является прекращение синтеза молекул белка, ДНК и РНК. [5]
О группе токсичных для бактерий белков ( колицинов) уже шла речь в разд. С этим же участком мембраны связывается антибиотик альбомицин. Существует предположение, что на ранних этапах эволюции у бактерий появились молекулы, обладающие способностью к образованию хелатных комплексов с железом, причем размер этих комплексов постепенно увеличился до такой степени, что они утратили способность диффундировать через наружную мембрану в клетку. В результате возникли специфические системы переноса, которые позднее были использованы фагами и; штаммами, продуцирующими колицинв. [6]
Группой Лурия было показано, что присоединение белковых молекул колицина К и Е1 к клеткам бактерии E-coli сопровождается прекращением синтеза макромолекул: белков, ДНК, РНК и гликогена. Прекращается также активный транспорт молочного сахара ( лактозы), глютамина, различных аминокислот и ионов калия и магния. В то же время клетка продолжает аккумулировать глюкозу, активный транспорт которой обеспечивается непосредственно энергией окисления молочной кислоты. [7]
В мутантной клетке, из-за отсутствия фермента АТФ-азы при присоединении молекулы колицина, гидролиз молекул АТФ в мембране не происходит. [8]
Вопрос о молекулярном механизме происходящих в мембране изменений при присоединении молекул колицина остается открытым. Возможно, что снижение разности потенциалов обусловлено конформационной перестройкой белковых молекул, участвующих в активном транспорте. [9]
Бактерия теряет способность к активному транспорту лактозы и глютамина ( рис. 32), когда молекула колицина проникает через цитоплазматическую мембрану. Одновременно внутри клетки резко уменьшается число молекул АТФ и прекращается синтез белков и молекул ДНК и РНК. [10]
Они называются так в связи с их свойством детерминировать образование культурами Escherichia coli особого рода антагонистических веществ - колицинов, способных поддерживать или выявлять антагонизм между родственными бактериями. Колицинами эти агенты назывались до тех пор, пока в качестве их продуцентов была известна только Escherichia coli. Позже, когда обнаружили, что аналогичные белковые вещества продуцируются и многими другими видами бактерий ( Shigella sonnei, Salmonella typhimu-rium, S. [11]
Для объяснения наблюдаемых эффектов влияния молекул колицина на нормальные и мутантные бактерии E-coli делается предположение, что внедрение молекулы колицина в клетку сопровождается снижением мембранной разности потенциалов. Снижение разности потенциалов приводит к прекращению активного транспорта лактозы, глютамина, ионов калия и магния через мембрану. В нормальной бактериальной клетке фермент АТФ-аза, находящийся в мембране в безнадежной попытке восстановить необходимую разность потенциалов, производит интенсивный гидролиз молекул АТФ, снижая количество этих молекул внутри клетки. Следствием уменьшения числа молекул АТФ является прекращение синтеза молекул белка, ДНК и РНК. [12]
Опыты с мутантными бактериями E-coli, лишенными фермента АТФ-азы в цитоплазматической мембране, показали, что при присоединении к ним молекул колицина их поведение существенно отличается от поведения обычной бактериальной клетки. После присоединения молекулы колицина к таким мутантным клеткам также происходит прекращение активного транспорта лактозы, глютамина и ионов К и Mg2, однако внутри клетки не прекращается синтез белков и молекул ДНК и РНК. При этом количество молекул АТФ внутри клетки даже возрастает. [13]
Они не обошли при этом вниманием бактериофаги, снабженные отростками: фаги Я, Т7 и Т4, а также плазмиду колицина Е-1. Преимущество этих систем состоит в том, что для них легче смоделировать репликацию ДНК в клеточных экстрактах, а кроме того, ДНК вирусов и плазмид хорошо изучены с генетической точки зрения. Во многих случаях репликация зависит как от генов вируса, так и от генов клетки-хозяина. Так, например, мутации генов dnaB, D, Е, F я G приводят к потере способности поддерживать рост фага Я точно так же, как и в случае, когда инактивированы / s - гены. Вместе с тем фаг К сохраняет способность к репликации в бактериях с мутантными генами Л и С. Многие вирусы, в том числе Т - четные фаги, содержат гены, кодирующие синтез своих собственных специфических ДНК-полимераз и других белков, необходимых для репликации. [14]
Разнообразные функции выполняют макромолекулы, локализованные частично или полностью на внешней стороне клеточной стенки, контактирующей с окружающей средой; это специфические рецепторы для фагов и колицинов; антигены ( липопо-лисахарид грамотрицательных эубактерии, тейхоевые кислоты грамположительных); макромолекулы, обеспечивающие межклеточные взаимодействия при конъюгации, а также между патогенными бактериями и тканями высших организмов. [15]
Страницы: 1 2