Количество - ампер-час
Cтраница 2
Теоретический расход энергии ( обозначенный через ТР) при получении 67 94 кг хлора равен произведению теоретического напряжения разложения ( 2 19 в) на количество затраченных ампер-часов. Это количество также можно определить как частное от деления количества вещества, полученного при электролизе, на химический эквивалент. [16]
 |
Зависимость плотности тока на ОРТА от концентрации хлоридов при межэлектродном расстоянии 3 мм fa и 6 мм ( б. [17] |
На производительность электролизеров и технико-экономические показатели их работы оказывают влияние такие режимные параметры как прикладываемое напряжение на разрядный промежуток, плотность тока межэлектродное расстояние, температура и расход электролита количество ампер-часов, затрачиваемое на 1 м3 обрабатываемой воды. [18]
В журнал должны вноситься: плотность электролита и напряжение всех элементов в конце разряда и в конце заряда; величины разрядного и зарядного тока; даты и время нахождения батареи в разряде и заряде; количество ампер-часов, отнятых от батареи при разряде и сообщенных ей при разряде; температура электролита в контрольных элементах во время заряда; плотность электролита в контрольных элементах ( ежедневно); результаты осмотров и измерений, данные о доливках; сведения о неисправностях аккумуляторов и о проведенных ремонтах. [19]
Так как процессы превращения энергии в аккумуляторе связаны с определенными потерями, то для заряда аккумулятора необходимо большее количество ампер-часов, чем то, которое аккумулятор отдает при разряде. Отношение количества ампер-часов, отдаваемого аккумулятором при разряде, к количеству ампер-часов, которое нужно соо. [20]
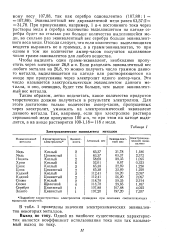 |
Электрохимические эквиваленты металлов. [21] |
Таким образом, легко подсчитать, какое количество продуктов теоретически должно получиться в результате электролиза. Для этого достаточно только количество ампер-часов, пропущенных через электролит, умножить на электрохимический эквивалент данного металла. Так, например, если при электролизе раствора сернокислой меди пропущено 100 а-ч, то при этом на катоде выделится, а на аноде растворится 100 - 1 18 118 г меди. [22]
При заряде щелочных аккумуляторов, в отличие от кислотных, отсутствуют объективные признаки конца заряда. Поэтому конец заряда определяется количеством ампер-часов, полученных аккумулятором от зарядной сети. [23]
Количество выделившегося при электролизе вещества прямо пропорционально силе тока и времени прохождения тока. Следовательно, количество получающегося при электролизе вещества зависит от количества ампер-часов ( а-ч), прошедших через электролит. [24]
Так как процессы превращения энергии в аккумуляторе связаны с определенными потерями, то для заряда аккумулятора необходимо большее количество ампер-часов, чем то, которое аккумулятор отдает при разряде. Отношение количества ампер-часов, отдаваемого аккумулятором при разряде, к количеству ампер-часов, которое нужно соо. [25]
На каждой стадии заряда ( кроме самой последней) наибольший ток, при котором еще не выделяются газы и не происходит быстрого повышения температуры, может быть определен из следующего приближенного правила, известного под названием правила ампер-часов. Зарядный ток, выраженный в амперах, не должен превосходить значения, численно равного разности между количеством ампер-часов, отнятых при предыдущем разряде, и количеством ампер-часов, уже возвращенных аккумулятору. Если, например, у батареи отнято при разряде 100 А - ч, то разряд может быть начат любым током, не превышающим 100 А. [26]
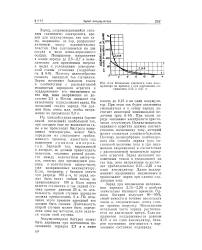 |
Изменение зарядного тока аккумулятора во времени / при постоянном напряжении 2 15 и 2 27 в. [27] |
На каждой стадии заряда ( кроме самой последней) наибольший ток, при котором еще не выделяются газы я не происходит быстрого повышения температуры, может быть определен из следующего приближенного правила, известного под названием правила ампер-часов. Зарядый ток, выраженный в амперах, не должен превосходить величины, численно разной разности между количеством ампер-часов, отнятых при предыдущем разряде, и количеством ампер-часов, уже возвращенных аккумулятору. Если, например, у батареи отнято при разряде 100 а-ч, то заряд может быть начат любым током, не превышающим 100 а. По истечении этого времени зарядный ток должен быть снижен. Длительность второй ступени может быть определена этим же методом, если задаться током этой ступени. [28]
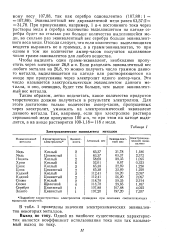 |
Электрохимические эквиваленты металлов. [29] |
Отсюда следует, что если количество выделяющихся веществ выражать не в граммах, а в грамм-эквивалентах, то при одном и том же количестве ампер-часов получится одинаковое число грамм-эквивалентов для любого вещества. [30]
Страницы: 1 2 3 4