Количество - карбонат - кальций
Cтраница 3
Механические примеси обладают слабой растворимостью в 12 % - й соляной кислоте ( от 6 90 до 12 77), причем главным компонентом растворяющейся части являются соединения железа ( пробы со скв. Исследованные пробы содержали очень малое ( менее 1 %) количество карбоната кальция. Проба скв, № 774 / 34 Вынгаяхинского месторождения, состоящая в основном из глинистых частиц, содержала гораздо большее ( 5 07 %) количество карбоната кальция. [31]
Запаянную трубку с содержимым заключают р стальной кожух, снабженный колпачком и прокладкой. В этот кожух предварительно вводят достаточное для нейтрализации всей содержащейся в трубке кислоты количество карбоната кальция в а тот случай, если трубка неожиданно разобьется. Затем прибавляют твердую углекислоту в количестве, необходимом для создания давления, которое требуется при той температуре, при которой проводится реакция. [32]
Измеряют объем или массу газа, выделяющегося при какой-либо химической реакции, и вычисляют массу вещества, выделившего этот газ. Например, измерив объем выделившейся СО2 при обработке известняка соляной кислотой, определяют количество карбоната кальция. [33]
Запаянную трубку с содержимым заключают в стальной кожух, снабженный колпачком и прокладкой. В этот кожух предварительно вводят достаточное для нейтрализации всей содержащейся в трубке кислоты количество карбоната кальция на тот случай, если трубка неожиданно разобьется. Затем прибавляют твердую углекислоту в количестве, необходимом для создания давления, которое требуется при той температуре, при которой проводится реакция. [34]
Индекс Ланжелье, таким образом, служит лишь качественным показателем склонности воды к тому или иному процессу и не является количественной характеристикой агрессивных свойств воды. Итак, агрессивные свойства воды характеризуются двумя величинами: карбонатной емкостью воды, равной количеству карбоната кальция, которое растворяется в единице объема данной воды при переходе к равновесному состоянию, и интенсивностью карбонатной агрессии, определяемой скоростью процесса растворения карбоната кальция в начальный момент контакта его с агрессивной водой. Эти величины, характеризующие агрессивные свойства воды с разных сторон, взаимно дополняют друг друга. Из двух вод одна может быть более агрессивной по одной из характеристик, а другая - по второй. [35]
Если капля ртути вернется на то место, на котором она находилась до перегрева, это укажет, что MgC03 доломита разложен полностью. Такой кратковременный перегрев с последующим охлаждением можно повторять и получать прежний объем, если только количество неразложившегося карбоната кальция невелико. [36]
При этом количество образующегося карбоната кальция в 2 раза превышает количество извести, затраченной на эту реакцию. В результате даже с учетом расхода части извести на осаждение Mg ( OH) 2 и Fe ( OH) 3 количество карбоната кальция в шламе обычно превышает количество затраченной извести. Следовательно, при обжиге шлама количество извести превышает ее расход на обработку воды, что подтверждается опытом работы промышленных установок. [37]
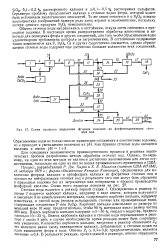 |
Схема процесса выделения фторида кальция. [38] |
Карбонат кальция измельчают до размера по меньшей мере 10 меш; предпочтительно, чтобы 90 % материала имело размер частиц 200 меш. Взвесь карбоната кальция и сточные воды перемешивают в реакторе 1 около 5 мин; в случае необходимости время реакции может быть сокращено или увеличено. Количество карбоната кальция, введенное в реактор обозначают Zi, эта величина равна числу эквивалентов кальция, добавленных к сточным водам на один эквивалент фтора в воде. [39]
Термическое разложение доломита исследовалось рядом авторов, но кинетика его в вакууме мало изучалась. Бриттон, Грегг и Винзор нашли, что в вакууме процесс происходит на поверхности раздела и что первичным продуктом реакции является ( Са, Mg) O, распадающийся вскоре на отдельные кристаллиты СаО и MgO; при разложении же в присутствии двуокиси углерода образуются СаСО3 и MgO. Однако даже в вакууме некоторое количество карбоната кальция получается за поверхностью раздела вследствие вторичного действия СО2 на окись кальция. Для доломита л0 67ч - 0 77 и Е составляет от 49 4 до 55 6 ккал. [40]
Что это, однако, не так, следует из опытов, проведенных с прибавлением и без прибавления карбоната кальция. В первом случае было найдено немного больше щелочных металлов, чем во втором; по всей вероятности это объясняется тем, что искусственно приготовленный тонкоизмельченный карбонат кальция лучше реагирует с хлоридом аммония, чем природный кристаллический карбонат кальция. Вполне достаточно, однако, брать половинное количество карбоната кальция по сравнению с тем, какое применяется в анализе силикатов. [41]
В данном случае гидроокись кальция - первичный катодный продукт - сразу реагирует с бикарбонатом, выделяя в осадок карбонат кальция. Последний реагирует затем с за-кисным бикарбонатом железа, образовавшимся под ним, переходя в закисный карбонат железа, и, наконец, если кислорода достаточно, - в гидрат окиси. Так, электрохимическое действие ведет к образованию пристающей ржавчины, часто содержащей некоторое количество карбоната кальция по всей поверхности, за исключением мениска, который остается катодным. [42]
Механические примеси обладают слабой растворимостью в 12 % - й соляной кислоте ( от 6 90 до 12 77), причем главным компонентом растворяющейся части являются соединения железа ( пробы со скв. Исследованные пробы содержали очень малое ( менее 1 %) количество карбоната кальция. Проба скв, № 774 / 34 Вынгаяхинского месторождения, состоящая в основном из глинистых частиц, содержала гораздо большее ( 5 07 %) количество карбоната кальция. [43]
Далее Блэк показал, что если оксид кальция оставить на воздухе, то он медленно превращается в карбонат кальция. Это было первое четкое указание на то, что воздух не простое вещество и, следовательно, вопреки представлениям древних греков он не является элементом в определении Бойля, а представляет собой смесь no - крайней мере двух различных веществ: обычного воздуха и углекислого газа. Изучая влияние нагревания на примере карбоната кальция, Блэк установил, как меняется вес вещества при нагревании. Он также определил, какое количество карбоната кальция нейтрализует заданное количество кислоты. [44]
 |
Технические характеристики химического поглотителя известкового ( ХП-И. [45] |
Страницы: 1 2 3 4