Количество - спектральная линия
Cтраница 1
Количество спектральных линий, относящихся к одному атому, достаточно велико. В настоящее время наши представления о строении любой химической частицы ( будь то атом, ион или молекула) настолько детальны, что сведения о практически всех ее спектральных линиях имеются в справочных изданиях. Для атомов и их ионов наибольшей популярностью пользуются диаграммы уровней энергий с указанием на них длин волн спектральных линий и сил осцилляторов соответствующих переходов. На рис. 1.2 приведен пример Гротриановской диаграммы для атома натрия. [1]
Таким образом, было обнаружено, что поистине необозримое количество спектральных линий описывается сравнительно простыми зависимостями, отличительной особенностью которых является наличие целочисленных параметров. [2]
Построить схему возможных переходов между 2D - и 2Р - состояниями в слабом магнитном поле и определить количество спектральных линий, которые при этом наблюдаются. [3]
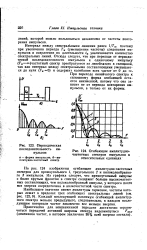 |
Огибающие амплитудно-частотных спектров импульсов в относительных единицах. [4] |
Интервал между спектральными линиями равен 1 / Т, поэтому при увеличении периода Тя ( уменьшении частоты) следования импульсов и сохранении их длительности / и увеличивается количество спектральных линий. Отсюда следует, что при переходе от периодической последовательности импульсов к одиночному импульсу ( Тиоо) частотный спектр преобразуется из линейчатого в сплошной, так как интервал между спектральными составляющими уменьшается до нуля ( FH 0) и содержит колебания всех частот от 0 до оо. [5]
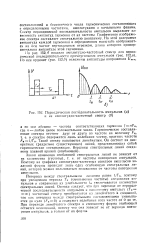 |
Периодическая последовательность импульсов ( а и ее амплитудно-частотный спектр ( б. [6] |
Интервал между спектральными линиями равен 1 / ТИ) поэтому при увеличении периода Гц ( уменьшении частоты) следования импульсов и сохранении их длительности / я увеличивается количество спектральных линий. Отсюда следует, что при переходе от периодической последовательности импульсов к одиночному импульсу ( Ти оо) частотный спектр преобразуется из линейчатого в сплошной, так как интервал между спектральными составляющими уменьшается до нуля ( f, 0) и содержит колебания всех частот от 0 до оо. При переходе линейчатого спектра к сплошному форма огибающей остается неизменной, потому что она зависит не от периода повторения импульсов, а только от их формы. [7]
Числовые значения этих функций называют спектральными термами. Таким образом, необозримое количество спектральных линий описывается сравнительно простыми зависимостями (14.1), (14.3), отличительной особенностью которых является наличие целочисленных параметров. [8]
Такое слабое поле влияет на состояние спиновой системы лишь в случае, если его частота о2 настроена точно на какую-либо линию спектра. Воздействие слабого поля является чисто локальным, и в результате никогда не наблюдается уменьшения количества спектральных линий. IV-48) получим, что ухЯафф у - Д - Уровни энергии ядра А расщепляются согласно уравнению IV-46 на величину V2Yx 2 и - а 2л / АХ, а спектральные линии - на величину Yx a. Так как ядерный спин может влиять на уровни энергии другого спина лишь при спин-спиновой связи между ними и квантование спина ядра X по направлению эффективного поля непосредствено влияет только на уровни энергии этого спина, то в спектре ядра А расщепляются лишь те линии, которые имеют общие уровни энергии со спином X. По мере повышения интенсивности возмущающего поля оно будет воздействовать и на другую линию дублета ядра X; при этом внутренние из четырех линий ядра А будут увеличиваться и сближаться, а внешние - уменьшаться и удаляться. [9]
Раскаленные атомарные газы и пары при низких давлениях дают линейчатый спектр, состоящий из отдельных цветных линий, разделенных темными промежутками. Каждое вещество в газообразном состоянии имеет свой линейчатый спектр с определенными цветом, положением и количеством спектральных линий. [10]
Наличие тонкой структуры указывает на более - сложное строение электронных уровней, чем то, ск которому приводит изложенная выше элементарная разработка теории Бора. Согласно последней, электроны движутся по рутовым орбитам, однозначно характеризуемым единственным главным квантовым числом п, и количество спектральных линий не должно превышать числа парных комбинаций этих чисел, отвечающих обеим орбитам, между которыми происходит переход электрона. Однако число линий в тонкой структуре значительно больше. [11]
Опытными данными установлено, что, в зависимости от характера аниона соли, окраска пламени получается различной. Так, например, при внесении на платиновой спирали в пламя бунзеновской горелки насыщенных растворов солей натрия, лития, калия, рубидия пли цезия количество спектральных линий не изменяется, а изменяется лишь их интенсивность. [12]
При термодинамическом равновесии форма линий поглощения совпадает с формой линий испускания. Благодаря тому, что спектральные линии не строго монохроматичны, а занимают некоторую полосу частот, дискретно - дискретные переходы могут оказывать значительное влияние на величину среднего по Росселанду пробега фотонов, так как количество спектральных линий для элементов с большим Z может быть огромным. [13]
Страницы: 1