Количество - бихромат
Cтраница 3
Сущность метода заключается в нагревании с обратным холодильником испытуемой пробы в концентрированной серной кислоте с известным количеством бихромата калия в присутствии серебряного катализатора в течение определенного промежутка времени. Затем проводят титрование остатка бихромата калия солью Мора и рассчитывают ХПК по количеству восстановленного бихромата. [31]
 |
Платиновый тигель, применяемый для определения закисного железа ( тигель Пратта. [32] |
Однако бихромат реагирует с плавиковой кислотой и степень протекания этой реакции, по-видимому, пропорциональна количеству избыточного бихромата. Поэтому следует отдать предпочтение методу Вильсона, где используется реакция с ванадатом аммония. [33]
Таким образом, количество бихромата, требуемое для полного окисления образца, складывается из бихромата, восстановленного до добавления серебра и после добавления. Разница соответствует содержанию уксусной кислоты в образце. Количество бихромата оценивают титрометри-чески. [34]
Стакан помещают в бане с охлаждающей смесью из мелко истолченного льда с солью ( примечание 1) и устанавливают в нем мешалку и термометр. Реакционную смесь охлаждают до температуры 2 С и, при перемешивании, начинают медленно ( по каплям) приливать раствор 30 г бихро-мата натрия в 75 мл воды ( примечание 2) с такой скоростью, чтобы температура реакции не превышала 5 С. После добавления всего количества бихромата смесь перемешивают еще в течение 15 мин и оставляют на ночь в холодильнике. На другой день в аналогичных условиях приливают вторую порцию бихромата ( 40 г Na2Cr2O7 в 120 мл воды), после чего перемешивают реакционную смесь еще в течение 0 5 ч ( примечание 3), а затем отсасывают выделившийся осадок сырого хинона на воронке Бюхнера. Осадок фильтруется медленно, поэтому фильтруют одновременно на двух воронках. [35]
 |
Влияние содержания.| Влияние содержания р-целлюлозы на прочность волокна ( по Бах-лотту. [36] |
При весовом методе определения устойчивости целлюлозу диспергируют в щелочи избранной концентрации, осадок отсасывают на воронке, быстро нейтрализуют уксусной кислотой, затем промывают водой и высушивают. При объемном методе определения в фильтрате или центрифугате определяют оксидиметрическим методом с К2Сг2О7 количество перешедшей в раствор целлюлозы, вернее, целлюлозы гемицеллюлозы. Этот метод позволяет быстро получить результат, но фактор пересчета количества израсходованного бихромата для целлюлозы ненадежен, так как он может значительно колебаться в зависимости от способа титрования и количества пентозанов. Поэтому указанный фактор необходимо устанавливать весовым путем для каждого типа целлюлозы и для каждого способа окисления. [37]
Раствор бихромата в разбавленной 1: 1 сериой кислоте весьма устойчив, но все же в какой-то мере он разлагается при кипячении. Поэтому каждый раз перед началом или в конце работы определяют нормальность бихромата в тех же условиях, в каких проводят окисление гумусовых веществ почвы. Такое определение ( обычно его называют холостым опытом) позволяет получить правильное представление о количестве бихромата, взаимодействующего с почвой, выразить это количество в мг-экв и вычислить содержание углерода в почве. [38]
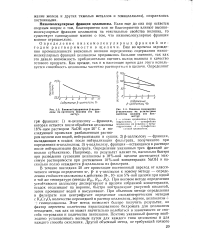
При действии - - излучения на растворы бихромата калия наблюдается восстановление иона бихромата до иона трехвалентного хрома. На рис. 8 приведены кривые зависимости количества восстановившегося бихромата калия от времени действия излучения. Для растворов, насыщенных кислородом и воздухом, и для обезгаженных растворов наблюдается линейная зависимость количества восстановленного бихромата от времени действия излучения. [39]
Измерение в области второго дает суммарное светопоглощение бихромата и перманганата, причем светопоглощение бихромата значительно больше. Поэтому вычитание величины, соответствую - щей определенному ( по данным первого фильтра) количеству перманганата, позволяет с достаточной точностью рассчитать количество бихромата. [40]
Эта окраска достаточно интенсивна и легко различима даже в присутствии окрашенного в зеленый цвет хрома ( III), который является продуктом восстановления бихромат-иона. Дифенилбензидин и дифенилбензидин фиолетовый легко переходят друг в друга, и именно эта обратимость реакции, стандартный потенциал которой равен 0 76 В относительно НВЭ, обеспечивает желаемое поведение индикатора. Как дифениламин, так и дифенилбензидин можно добавлять к титруемому раствору, но дифенилбензидин более предпочтителен, так как при его окислении в дифенилбензидин фиолетовый расходуется всего половина количества бихромата, необходимого для окисления дифениламина в фиолетовую форму. [41]
Затем нагревают еще 15 минут. Во время всей операции отгоняется некоторое количество воды, непрореагировавшего спирта и изовалерианового альдегида. В дестиллате отделяют маслянистый слой от водного и перегоняют первый с хорошей колонкой, причем между 90 и 94 получается альдегидная фракция, а при соответствующей температуре перегоняется неизмененный изоамиловый спирт, так как применявшееся количество бихромата недостаточно для окисления. Кон выразительно подчеркивает, что очистка изовалерианового альдегида через бисульфитное соединение оказалась весьма непрактичной. Ван Марле и Толленс, невидимому, в свою очередь не знали работы Кона или не обратили на нее внимания. [42]
Затем нагревают еще 15 минут. Во время всей операции отгоняется некоторое количество воды, непрореагировавшего спирта и изовалерианопого альдегида. В дестил-лито отделяют маслянистый слой от одного и перегоняют первый с хорошей колонкой, причем между 90 и 94 получается альдегидная фракция, а при соответствующей температуре перегоняется неизмененный ИЗОЭМИЛОБГЛЙ спирт, так как применявшееся количество бихромата по достаточно для окисления. [43]
Титрование производится следующим образом: к 20 мл пробы в конической колбе прибавляют 2 л H2S04 и 3 мл KJ 15-процентного, закрывают пробкой и оставляют на 5 мин. Затем прибавляют 20 мл воды и титруют N / 100 раствором серноватокислого натрия. Сначала титруют 20 мл N / 100 раствора бихромата, чтобы определить поправку растворов. Затем титруют 20 мл контрольного опыта и полученный результат перечисляют на весь объем контрольного опыта; наконец титруют 20 мл пробы и результат также перечисляют на объем всей пробы. Полученное количество вычитают из контрольного опыта и узнают количество бихромата, прореагировавшего со свинцом. Умножают это количество на поправку раствора. N / 100 бихромата соответствует 0 69 мг свинца; отсюда вычисляют количество свинца в определяемой пыли. [44]
Титрование производится следующим образом: к 20 мл пробы в конической колбе прибавляют 2 л Н2 SO4 и 3 мл KJ 15-процентного, закрывают пробкой и оставляют на 5 мин. Затем прибавляют 20 мл воды и титруют N / 100 раствором серноватокислого натрия. Сначала титруют 20 мл N / 100 раствора бихромата, чтобы определить поправку растворов. Затем титруют 20 мл контрольного опыта и полученный результат перечисляют на весь объем контрольного опыта; наконец титруют 20 мл пробы и результат также перечисляют на объем всей пробы. Полученное количество вычитают из контрольного опыта и узнают количество бихромата, прореагировавшего со свинцом. Умножают это количество на поправку раствора. N / 100 бихромата соответствует 0 69 мг свинца; отсюда вычисляют количество свинца в определяемой пыли. [45]
Страницы: 1 2 3