Катодная добавка
Cтраница 2
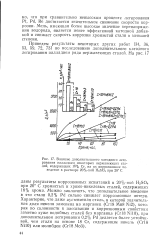 |
Влияние дополнительного катодного легирования палладием некоторых нержавеющих сталей, содержащих 18 % Сг, на их коррозионное поведение в растворе 20 % - ной H3SC4 при 20 С. [16] |
Медь, имеющая более высокое значение перенапряжения водорода, является менее эффективной катодной добавкой и снижает скорость коррозии хромистой стали в меньшей степени. [17]
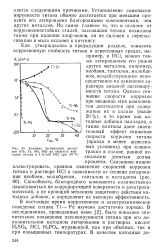 |
Влияние легирующих металлов ( Mb, Та, Mo, Pd на скорость коррозии титана в 5 % - ной НС1 при 100 С. [18] |
Способность благородного компонента количественно накапливаться на корродирующей поверхности и электрохимический, а не кроющий механизм защитного действия катодных добавок, и определяют их высокую эффективность. В настоящее время коррозионное и электрохимическое поведение сплава Ti - Pd изучено достаточно хорошо. В исследованиях, проведенных нами [2], было показано значительное повышение пассивируемости титана при его дополнительном катодном легировании в растворах кислот H2SO4, HC1, Н3РО4, муравьиной, как при обычных, так и при повышенных температурах. [19]
Если у металла или сплава потенциал пассивации более отрицательный, чем потенциал катодного процесса водородной деполяризации на сплаве с катодной добавкой, то вполне возможна пассивация сплава за счет водородной деполяризации. Из этих кривых видно, что перенапряжение водорода при введении в титан 1 % Pt снижается на 350 - 400 мв. Вследствие этого стационарный потенциал сплава титана с платиной смещается в положительную сторону, в область пассивных значений, где процесс анодного растворения титана сильно заторможен. Это обеспечивает высокую коррозионную стойкость сплава титана с платиной. [20]
Поскольку в литературе подобных данных для титана нет, а эти данные важны для понимания механизма коррозии сплавов титана с катодными добавками, была проведена работа по изучению влияния гальванического контакта некоторых металлов с низким значением перенапряжения водорода на анодное поведение титана в растворах серной кислоты. [21]
Практически важные сплавы, например, на основе титана, тантала, ниобия, хрома, коррозионностойкие стали, модифицированные катодными добавками палладия, рутения, платины и др. могут служить иллюстрацией подобных коррозионных систем. [22]
Причем она зависит не только от стационарного потенциала чистых добавок и их коррозионной стойкости, а также от изменения перенапряжения на этих катодных добавках под влиянием насыщения их водородом. [23]
Одновременное легирование сплава компонентами, тормозящими анодный процесс ( пассивирующие добавки), и ком -, понентами, облегчающими протекание катодного процесса ( катодные добавки), часто является наиболее эффективным методом получения сплава повышенной коррозионной стойкости. [24]
Титан, который обладает высокой пассивируемостью в ряде сред, особенно интересен в этом отношении, поскольку его потенциал полной пассивации очень сильно смещен в отрицательную сторону, что особенно благоприятствует созданию сплавов с катодными добавками. Поскольку действие таких добавок связывается с их влиянием в основном на катодный процесс [2] и поскольку работу такой системы можно рассматривать как работу гальванической пары Ti ( анод) - легирующая добавка ( катод), было интересно исследовать поведение титана в гальванических парах с чистыми катодными металлами, изучить и сравнить катодное поведение этих металлов, а также выявить роль различных катодных характеристик ( перенапряжение водорода, предельный диффузионный ток по кислороду, перенапряжение ионизации кислорода, собственный стандартный потенциал добавки) в процессах пассивации титана в результате контакта с катодными металлами. [25]
После обоснования электрохимического механизма коррозии как результата работы коррозионного элемента, предло - женного сначала в общем виде Де ла Ривом [28], а затем развитого Уитни [29], Пальмером [30], Эвансом [31], Акимовым [5], в течение ряда лет господствовало мнение, что всякое увеличение эффективности катодного процесса, например контакт с более электроположительными металлами, нанесение катодного несплошного покрытия, легирование металла катодной добавкой или даже введение достаточно положительных ионов в раствор, должно вызвать ускорение процесса электрохимической коррозии. [26]
При легировании стали рением сильно снижается перенапряжение выделения водорода и коррозионная стойкость возрастает вследствие смещения потенциала стали в положительную сторону, в область пассивных значений. Рений-является эффективной катодной добавкой, аналогичной палладию и платине. [27]
 |
Значение параметров поляризационных кривых для легированных покрытий. [28] |
Благоприятное действие дооавок кремния и титана на коррозионную стойкость алюминиевых покрытий на стали заключается в появлении новой, отличной от чистого алюминия структуре. Вследствие этого подобные покрытия можно рассматривать как алюминиевые с катодной добавкой, что подтверждается характером изменения стационарного потенциала с ростом содержания кремния. С увеличением плотности тока на анодных участках и степени облагораживания потенциала облегчается возможность перехода анодных участков в пассивное состояние. [29]
Наоборот, для условий, в которых возможна пассивация сплава, наибольший эффект будет получен от легирующих компонентов, повышающих эффективность катодного процесса. Наиболее эффективным методом получения сплава повышенной коррозионной стойкости часто является одновременное легирование пассивирующими и катодными добавками. При этом возможно повышение коррозионной стойкости сплава увеличением общей термодинамической стабильности сплава. [30]
Страницы: 1 2 3