Количество - выделяющееся вещество
Cтраница 2
Формулы (2.1) - (2.4) по своему построению идентичны: каждая из них представляет дробь, числитель которой выражает количество выделяющегося вещества, а знаменатель - ассимилирующую-способность 1 м3 вентиляционного воздуха. [16]
Продукты разложения электролита, например, водород и кислород в опыте, описанном в § 40, выделяются на электродах все время, пока идет ток, и их количества можно измерить. Но особенно легко измерять количество выделяющегося вещества, если подобрать такой раствор. Так, если пропускать ток через раствор медного купороса ( CuSO4), то на катоде откладывается медь. Это явление легко наблюдать, если сделать катод, например, из угля; на черной поверхности угля ясно заметен красноватый слой выделившейся меди. Взвешивая катод до и после опыта, можно точно определить массу осадив-шегося металла. [17]
Продукты разложения электролита, например, водород и кислород в опыте, описанном в § 40, выделяются на электродах все время, пока идет ток, и их количества можно измерить. Но особенно легко измерять количество выделяющегося вещества, если подобрать такой раствор, при котором выделяющееся вещество оседает в виде твердого осадка на электроде. Так, если пропускать ток через - раствор медного купороса ( CuSO4), то на катоде откладывается медь. Это явление легко наблюдать, если сделать катод, например, из угля; на черной поверхности угля ясно заметен красноватый слой выделившейся меди. Взвешивая катод до и после опыта, можно точно определить массу осадившегося металла. [18]
Продукты разложения электролита, например, водород и кислород в опыте, описанном в § 40, выделяются на электродах все время, пока идет ток, и их количества можно измерить. Но особенно легко измерять количество выделяющегося вещества, если подобрать такой раствор, при котором выделяющееся вещество оседает в виде твердого осадка на электроде. Так, если пропускать ток через раствор медного купороса ( CuSO4), то на катоде откладывается медь. Это явление легко наблюдать, если сделать катод, например, из угля; на черной поверхности угля ясно заметен красноватый слой выделившейся меди. Взвешивая катод до и после опыта, можно точно определить массу осадив-шегося металла. [19]
По-видимому, наиболее обычен случай лишь частичного распада соединения и выделения некоторой доли его в неизмененном виде. При этом соотношение между количествами выделяющегося вещества и, напротив, подвергающегося биотрансформациям в той или иной степени зависит от концентрации вдыхаемого яда или от попавшей в организм иным путем дозы его. [20]
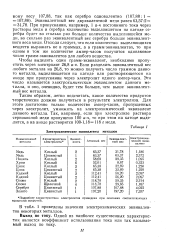 |
Электрохимические эквиваленты металлов. [21] |
Отсюда следует, что если количество выделяющихся веществ выражать не в граммах, а в грамм-эквивалентах, то при одном и том же количестве ампер-часов получится одинаковое число грамм-эквивалентов для любого вещества. [22]
Законы Фарадея соблюдаются во всех случаях и при любых условиях ведения электролиза. Если вещество выделится в количестве меньшем, чем то, которое может быть найдено по расчету в соответствии с временем электролиза и силой тока, то это может означать только, что затрачиваемое количество электричества используется непроизводительно. Наряду с выделением данного вещества может иметь место и побочный процесс. Например, выделение водорода, как это и бывает при электролитическом получении металлов из водных растворов. Количество выделяющегося вещества может быть значительно снижено или даже сведено к нулю, если не воспрепятствовать там, где это необходимо, обратному воссоединению катодных и анодных продуктов в исходное вещество. Это может иметь место, например, при получении металлов электролизом их расплавленных хлоридов. В этом случае применяют электролизеры специального устройства, обеспечивающие надежную защиту полученного металла от выделяющегося на аноде хлора. [23]
Страницы: 1 2