Количество - данное вещество
Cтраница 3
Титрование - это основной метод объемного химического анализа, заключающийся в постепенном добавлении титрованного раствора к раствору вещества, количество которого необходимо определить. По объему израсходованного титрованного раствора вычисляется количество данного вещества. Изменение величины рН в зависимости от количества добавленной кислоты ( щелочи) можно изобразить графически в виде кривой титрования. Однако довольно часто мы анализируем системы, существующие только на бумаге, и в этих случаях вынуждены производить громоздкие расчеты. [31]
Процедуру градуировки повторяют 5 раз. Для каждого из анализируемых веществ сравнивают коэффициенты Ki при разных соотношениях количеств данного вещества и внутреннего стандарта в пробе. [32]
Особенно важное значение имеет - изменение чувствительности различных реакций в присутствии посторонних веществ. Шоорль, впервые обративший внимание jia это обстоятельство, предложил назвать п ред-ельным отношением отношение количества данного вещества, которое еще может быть открыто в присутствии постороннего вещества, к количеству последнего. Сведения о предельных отношениях для различных реакций на один и тот же ион позволяют, отобрать наиболее специфический метод обнаруже ния открываемого иона в присутствии посторонних ионов. [33]
Микрокулонометрический метод анализа обеспечивает абсолютное и стехиометрическое определение количества хлора, серы, азога или фосфора, поступающего в ячейку для титрования. Если известна формула анализируемого вещества, то по вычисленному количеству одного из этих элементов можно определить количество данного вещества, присутствующее в анализируемой пробе. [34]
Энтальпия - это функция состояния системы, равная величине внутренней энергии ( U), сложенной с произведением объема на давление: Н / PV. Внутренняя энергия системы, есть параметр состояния; она характеризует запас энергии системы и зависит от вида и количества данного вещества и от условий его существования; она прямо пропорциональна его количеству. [35]
Составим материальный баланс для вещества В. Количество вещества В в емкости Ур после реакции равно количеству вещества В, полученного в результате реакции, минус количество данного вещества, ушедшего из реакции с раствором. [36]
Его можно относить к любому количеству вещества, при условии, что теплота перехода и соответствующее изменение объема отнесены к одному и тому же количеству данного вещества. [37]
Если в воздухе находится только одно вещество, то количество углерода можно пересчитать на данное вещество. Если это вещество химически неоднородное, а представляет собой смесь углеводородов, как, например, бензин, керосин, то, чтобы получить коэффициент для пересчета углерода на данное вещество, нужно сжечь некоторое количество его и вычислить, какому количеству данного вещества соответствует 1 мг углерода ( стр. Иногда, при наличии смеси, пересчитывают количество углерода на то вещество, которое преобладает в данной смеси. [38]
Для органической химии возможность осуществления препаративного газохроматографического разделения имеет, пожалуй, большее значение, чем для всех остальных областей химии. В лаборатории автора в препаративных целях проводится почти половина всех газохроматографических разделений. Проводимое разделение можно характеризовать тем количеством данного вещества, которое требуется получить. Наиболее распространено разделение относительно простых смесей, в которых требуемые количества разделенных компонентов измеряются миллиграммами и которое осуществляют с целью дальнейшего анализа разделенных веществ при помощи спектроскопии в ультрафиолетовой, видимой или инфракрасной областях спектра, масс-спектроскопии или спектроскопии ЯМР. Многие проблемы препаративной хроматографии смесей органических веществ связаны с другой задачей, когда требуется получить несколько большие количества этих веществ ( 50 мг) или когда разделяемая смесь состоит из большого числа компонентов. Наконец, иногда возникает необходимость получения еще больших количеств разделенных веществ в чистом виде ( миллилитр), и это также требует применения специальных методов. [39]
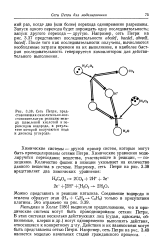 |
Сеть Петри, представляющая окислительно-восстановительную реакцию между щавелевой кислотой и пе-роксидом водорода, в результате которой получаются вода и диоксид углерода. [40] |
Химические системы - другой пример систем, которые могут быть промоделированы сетями Петри. Химические уравнения моделируются переходами; вещества, участвующие в реакции, - позициями. Количество фишек в позиции указывает на количество данного вещества в системе. [41]
Для обозначения концентрации применяется следующее правило. Выражение соляная кислота ( 1 3) означает, что в 2 см3 воды растворен 1 см3 соляной кислоты. Указание концентрации растворов твердых реактивов в процентах означает безводное количество данного вещества в граммах, содержащееся в 100см3 раствора. [42]
Наряду с высокой чувствительностью ( 10 - 9 г по хлору, сере, азоту и фосфору) детектор чрезвычайно селективен. В большинстве случаев микрокулонометрический метод анализа обеспечивает абсолютное и стехиометрическое определение количеств хлора, серы, азота или фосфора, поступающих в ячейку. Причем, если известна формула соединения, то по найденному количеству одного из этих элементов можно определить количество данного вещества. [43]
Сам по себе процесс электровосстановления был известен еще Дэви и Фарадею: именно методом катодного восстановления были получены натрий, литий и многие другие металлы. Капилляр, придуманный для измерения поверхностного натяжения капающей ртути, неожиданно оказался идеальным электродом, на котором результаты повторяемых измерений потенциала оказались сходными, как две капли ртути. И не только нахождения, но и точного измерения их количества: выяснилось, что высота ступеньки прямо пропорциональна количеству данного вещества в растворе. [44]
 |
Полярографическая ячейка для непрерывного амперометри-ческого определения концентрации в эффлюенте. [45] |
Страницы: 1 2 3 4