Чистые амин
Cтраница 1
Чистые амины представляют собой твердые, воскообразные вещества, которые перед применением необходимо диспергировать. [1]
 |
Давление насыщенных паров водных растворов этаноламинов ( ЭА различной концентрации. [2] |
При обычных температурах все чистые амины кроме ДГАи МДЭА являются твердыми веществами. Добавление воды в амины приводит к снижению температуры застывания и вязкости растворов, благодаря чему становится возможным вести процесс очистки газа при относительно низких положительных температурах. [3]
Заметим сразу, что действие чистых аминов не ограничивается лишь подщелачиванием коррозионной среды. Если в присутствии гексаметиленимина анодный процесс был в широком интервале потенциалов полностью подавлен, то в электролите с аналогичным значением рН, но в отсутствие органических катионов скорость анодной реакции практически не изменилась. Это указывает на то, что органический катион влияет на процесс анодного растворения. [4]
Следует подчеркнуть, что во всех исследованиях использовались чистые амины, а не их соли. [5]
Характерным свойством исследованных соединений является возрастание их защитных свойств по мере перехода от чистых аминов к бензоатам, нитробензоатам и динитро бензо-атам. [6]
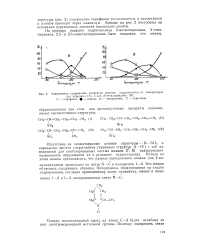 |
Зависимость содержания продуктов реакции гидрогенолиза от температуры. [7] |
Отсутствие на хроматограмме аминов структуры - R - NH2 и совпадение времен удерживания указанных структур ( I-IV) с той же величиной для синтезированных чистых аминов [7, 8] подтверждает возможность образования их в реакциях гидрогенолиза. [8]
Многие сульфамиды первичных и вторичных аминов могут быть разделены посредством обработки их щелочью, и поэтому гидролиз этих соединений представляет интерес как способ получения чистых аминов. Однако сульфамиды значительно менее гидролизуются, чем амиды карбоновых кислот. [9]
 |
Зависимость содержания продуктов реакции гидрогенолиза от температуры. [10] |
Отсутствие на хроматограмме аминов структуры - R - NH2 и совпадение времен удерживания указанных структур ( I - IV) с той же величиной для синтезированных чистых аминов [7, 8] подтверждает возможность образования их в реакциях гидрогенолиза. [11]
На рис. 22 показано влияние времени предварительной выдержки стального электрода в атмосфере летучих ингибиторов на начальное значение электродного потенциала стали. Как видно, с увеличением времени выдержки потенциал электрода заметно сдвигается в положительную сторону; наибольший сдвиг вызывают чистые амины, их соли слабее изменяют потенциал. Объясняется это более высоким давлением паров аминов по сравнению с давлением паров И Х солей. [12]
Например, когда в ацетоновую среду, содержащую йодистый метил, впрыскивают смесь н-бутиламин - трибутиламин ( 71 % н-бутиламина), общая константа скорости реакции К оказывается меньше ожидаемой из-за медленного образования шиффовых оснований. Кривая 1 на рис. 36 показывает, что значение / С для этой смеси не постоянно, а уменьшается со временем. Константы скорости для чистых аминов были измерены при отношении концентраций реагента [ Rb / [ Rb2, которое немного ниже чем / е - оптимальное время измерения. При этом заниженные результаты получаются из-за того, что в случае чистого н-бутиламина кажущаяся константа скорости реакции второго порядка все же больше, чем таковая, полученная при анализе смеси. Например, вследствие того, что равновесие реакций, протекающих по уравнениям ( 138а) и ( 1386), достигается медленно, измеренные при времени, равном / е, константы скорости реакций второго порядка с участием н-бутиламина будут уменьшаться с уменьшением концентрации свободного н-бутиламина. [13]
Страницы: 1