Количество - кристаллизационная вода
Cтраница 2
Определим содержание каинита по количеству выделенной кристаллизационной воды. [16]
Мета-вольфрамат натрия кристаллизуется с колеблющимися количествами кристаллизационной воды и также содержит конституционную воду. На воздухе соль легко выветривается; при сушке над серной кислотой, по данным Форхера, теряет большую часть, а по наблюдениям Фридгейме [ в ] - лишь половину своей кристаллизационной воды. [17]
Если имеются сомнения о количестве кристаллизационной воды в препарате, раствор доводят ДО удельного веса 1 270 при температуре 20 С. [18]
Кристаллогидраты солей различаются и по количеству кристаллизационной воды, и по характеру связи молекул воды с другими частицами, составляющими кристалл. Нередко данное соединение образует несколько кристаллогидратов, различающихся по содержанию воды. При этом кристаллогидрат с наибольшим содержанием воды устойчив при относительно более низких температурах, а с повышением температуры он становится неустойчивым и разлагается с образованием менее гидратированного продукта. Так, СаС12 образует четыре кристаллогидрата. Наиболее богатый водой гексагидрат СаС12 6Н2О устойчив до 30 1 С. При этой температуре он плавится в своей кристаллизационной воде. [19]
Кристаллогидраты солей различаются и по количеству кристаллизационной воды, и по характеру связи молекул воды с другими частицами, составляющими кристалл. Нередко данное соединение образует несколько кристаллогидратов, различающихся по содержанию воды. При этом кристаллогидрат с наибольшим содержанием воды устойчив при относительно более низких температурах, а с повышением температуры он становится неустойчивым и разлагается с образованием менее гидратированного продукта. Так, СаС12 образует четыре кристаллогидрата. Наиболее богатый водой гексагидрат СаС12 6Н2О устойчив до 30 1 С. При этой температуре он плавится в своей кристаллизационной воде. [20]
Кристаллогидраты солей различаются и по количеству кристаллизационной воды, и по характеру связи молекул воды с другими частицами, составляющими кристалл. Нередко данное соединение образует несколько кристаллогидратов, различающихся по содержанию воды. При этом кри сталлогидрат с наибольшим содержанием воды устойчив при от носительно более низких температурах, а с повышением темпера туры он становится неустойчивым и разлагается с образованием менее гидратированного продукта. Так, СаСЦ образует четыре кристаллогидрата. Наиболее богатый водой гексагидрат СаСЬ 6Н2О устойчив до 30 1 С. При этой температуре он плавится в своей кристаллизационной воде. [21]
 |
Структура льда ( заштрихованные круги представляют водородные атомы данной молекулы. черные - связи ее кислорода с водородными атомами соседних молекул. [22] |
Кристаллогидраты солей различаются и по количеству кристаллизационной воды, и по характеру связи молекул воды с другими частицами, составляющими кристалл. [23]
Значение этой величины позволяет Судить о количестве растворенной и кристаллизационной воды в данном материале. [24]
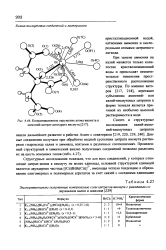 |
Координационное окружение атома висмута в аммоний-цитрат-дигидрате висмута. [25] |
При замене аммония на калий меняется только количество кристаллизационной воды и происходят незначительные изменения пространственного расположения структуры. По мнению авторов [217, 218], агрегация субъединиц аммоний - или калий-висмутовых цитратов в форме тоннеля является причиной их необычно высокой растворимости в воде. [26]
 |
Относительное расположение ионов металла и молекул воды в гидратах катионов ( а Li - 4H2O и ( б Mg2 - 6H2O - no Берналу. [27] |
Особо нужно отметить кристаллогидраты солей, в которых количество кристаллизационной воды превосходит количество самой соли. Все они устойчивы только при невысоких температурах. [28]
 |
Относительное расположение ионов металла и молекул воды в гидратах катионов ( а Li - 4H2O и ( б Mg2 - 6H2O - no Берналу. [29] |
Особо нужно отметить кристаллогидраты солей, в которых количество кристаллизационной воды превосходит количество самой соли, Все они устойчивы только при невысоких температурах. Такие кристаллогидраты называют тектогидратами. [30]
Страницы: 1 2 3