Количество - грамм-эквивалент
Cтраница 3
Определить нормальную концентрацию 16 % - кого раствора сульфата меди - это значит найти количество грамм-эквивалентов вещества, содержащегося в 1000 мл данного раствора. [31]
Природа щелочи в этом случае роли не играет, так как из данных рассчитывается лишь количество грамм-эквивалентов ее, участвующее в реакции нейтрализации. [32]
 |
Мерная посуда. [33] |
Так как 1 г-экв известного реактива вступает в реакцию с 1 г-экв анализируемого вещества, то количество грамм-эквивалентов реактива, вступившего в реакцию, равное AfpVp, и количество грамм-эквивалентов прореагировавшего исследуемого вещества NttVB должны быть равны между собой: Л рУр Л ВУВ. [34]
Так как сильноосновные аниониты в схемах полного химического обессоливания предназначены для обес-кремнивания, их обменная способность характеризуется рабочей кремнеемкостью, выраженной количеством грамм-эквивалентов HSiO3, которое может извлечь из воды 1 м3 набухшего анионита в результате обменной реакции. [35]
Так как сильноосновные аниониты в схемах полного химического обессоливания предназначены для обескдед-нивания, их обменная способность характеризуется рабочей кремнеемкостью, выраженной количеством грамм-эквивалентов HSiO3 -, которое может извлечь из воды 1 м3 набухшего анионита в результате обменной реакции. Рабочая кремнеемкость сильноосновных анионитов зависит от величины рН воды, поступающей на анионит-ный фильтр, концентрации кремниевой кислоты в этой воде, удельного расхода щелочи на регенерацию, концентрации регенерирующего раствора, момента отключения фильтра на регенерацию, скорости фильтрования воды, природы обменного иона ( ОН -, НСО3 -, СО32 -), температуры исходной воды и других факторов. [36]
Законы Фарадея не указывают, какое из веществ в растворе подвергается при электролизе изменению, а только выражают зависимость между прошедшим количеством электричества и количеством грамм-эквивалентов всех веществ, претерпевающих химические изменения в результате электролиза. [37]
Законы Фарадея не указывают, какое из веществ в растворе подвергается при электролизе изменению, а только выражают зависимость между прошедшим количеством электричества и количеством грамм-эквивалентов всех веществ, претерпевающих химические изменения в результате электролиза. Следовательно, при применении законов Фарадея должны быть учтены как главные, так и побочные процессы. [38]
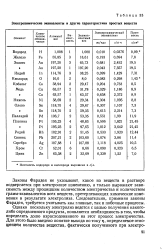 |
Электрохимические эквиваленты и другие характеристики простых веществ. [39] |
Законы Фарадея не указывают, какое из веществ в растворе подвергается при электролизе изменению, а только выражают зависимость между прошедшим количеством электричества и количеством грамм-эквивалентов всех веществ, претерпевающих химические изменения в результате электролиза. Следовательно, применяя законы Фарадея, требуется учитывать как главные, так и побочные процессы. [40]
Законы Фарадея не указывают, какое из веществ в растворе подвергается лри электролизе изменению, а только выражают зависимость между прошедшим количеством электричества и количеством грамм-эквивалентов всех веществ, претерпевающих химические изменения в результате электролиза. [41]
Возвращаясь к схеме перемещения ионов, обозначим скорости движения их через uk ( катион) и иа ( анион), а через ak и аа количество грамм-эквивалентов, перешедших йюсле электролиза в катодное и анодное пространство. [42]
Жду Двумя электродами, находящимися ни расстоянии /, F - число Фарадея, и и и - - подвижности катиона и аниона, с - количество грамм-эквивалентов катионов или анионов в I л взятого раствора. [43]
По количеству выделенного иода можно вычислить титр кислоты ( в г / мг), введенной в раствор, так как выделенное количество иода точно равно количеству прореагировавших грамм-эквивалентов ионов водорода. [44]
Так как 1 г-экв известного реактива вступает в реакцию с 1 г-экв анализируемого вещества, то количество грамм-эквивалентов реактива, вступившего в реакцию, равное AfpVp, и количество грамм-эквивалентов прореагировавшего исследуемого вещества NttVB должны быть равны между собой: Л рУр Л ВУВ. [45]
Страницы: 1 2 3 4