Количество - двуокись - сера
Cтраница 3
 |
Примерный состав колчеданов, применяемых для производства серной кислоты. [31] |
Например, при получении 1 т черновой меди одновременно образуется 7 3 т SOa. Из этого количества двуокиси серы можно получить примерно 11 т серной кислоты. [32]
Интересно выяснить, как будет изменяться влияние процессов переноса к внешней поверхности зерен катализатора при изменении состава газа, в частности при повышении концентраций реагирующих компонентов. Как видно из уравнения ( VI, 14), количество G двуокиси серы, окисляемой на единице наружной поверхности зерен, не зависит от начальной концентрации двуокиси серы и прямо пропорционально концентрации кислорода. [33]
Интересно выяснить, как будет изменяться влияние процессов переноса к внешней поверхности зерен катализатора при изменении состава газа, в частности при повышении концентраций реагирующих компонентов. Как видно из уравнения ( VI, 14), количество G двуокиси серы, окисляемой на единице наружной поверхности зерен, не зависит от начальной концентрации двуокиси серы и прямо пропорционально концентрации кислорода. Разность между концентрациями двуокиси серы в объеме и у поверхности зерен, как следует из уравнения ( VI, 15), пропорциональна G и, следовательно, пропорциональна также концентрации кислорода и не зависит от начальной концентрации двуокиси серы. [34]
Затем прибавляют 20 весовых частей уксусного ангидрида, содержащего эквивалентное находящемуся в уксусной кислоте количеству хлора количество двуокиси серы, и размешивают в течение 1 часа при комнатной температуре. Затем температуру поднимают до 55 и продолжают размешивание до тех пор, пока не образуется прозрачный раствор ( около 4 час. Выливанием в большое количество воды, неоднократным растиранием пыпДОгаего продукта с водой и сушкой растиранием со спиртом и затем с эфиром получают чисто белый порошок / выходом 96 % от теории, свободный от следов SOS и С12 и легко растворимый в хлороформе и ацетоне; a) D 170 в хлороформе. Ацегилирование можно производить также при более низкой температуре, однако в этом случае оно продолжается соответственно дольше и ведет к слишком вязкому продукту, который в общем идентичен с описанным. [35]
Поскольку система содержит летучий компонент, сначала определялась диаграмма температура-давление, когда в системе находились в равновесии три фазы: твердая, жидкая и газообразная. Это необходимо для того, чтобы при определении диаграммы плавкости ввести поправку ( при вычислении молекулярного соотношения компонентов) на количество двуокиси серы, оставшейся в газовой фазе. [36]
Экстрагирование образца сульфидированной древесины пиридином давало 89 3 % остатка древесины с 22 8 % лигнина, 4 54 % метоксилов и 1 59 % серы. Древесина, подвергнутая варке только с забуференным раствором и сульфидированная древесина были подвергнуты варкам с бисульфитным щелоком, содержавшим 0 94 г бисульфита натрия и варьирующие количества двуокиси серы на 100 мл. [37]
Количество подаваемого воздуха регулируют винтовым зажимом, температуру в слое - реостатами. Подачу двуокиси серы для получения газовой смеси заданного состава начинают при 400 - 450 С. Количество двуокиси серы замеряют реометром. Точный состав газовой смеси, поступающей в контактный аппарат, определяют анализом. Температура в аппарате поддерживается в пределах 400 - 600 С в зависимости от заданных условий. [38]
Если количество двуокиси серы в газе ниже 0 1 %, то количество серы в окалине и металле невелико, однако оно весьма быстро увеличивается вместе с содержанием серы в газе. Это согласуется с гипотезой о том, что слабо защитный характер окалины, получающейся в присутствии серы, объясняется пористостью слоя вторичных окислов, которые образуются вследствие разложения сернистых соединений. При низких концентрациях двуокиси серы разложение сульфатов ( или сульфитов) идет с такой же быстротой, как и их образование; сравнительно весьма небольшое количество серы, которое обнаруживается в окалине, может дать большое ускорение коррозионного воздействия. При более высоких концентрациях серы сернистые соединения начинают накапливаться в окалине, и в этих условиях дальнейшее увеличение двуокиси серы в газовой фазе мало влияет на повышение скорости окисления. [39]
При этом в жидкой двуокиси серы растворяются ароматические соединения, некоторая часть нафтенов и другие соединения, неблагоприятно отражающиеся на сульфохлорировании. Вещества эти в качестве экстракта удаляются, а очищенный продукт ( рафинат) обогащается парафинами, что видно из значительного уменьшения удельного веса. В зависимости от количества двуокиси серы и углеводородов нефти, а также от температуры экстрагирования получают различные количества экстракта. [40]
Угольный измерительный электрод 1 имеет потенциал более положительный на величину наложенного напряжения. При этом потенциале двуокись серы, подводимая к измерительному электроду, окисляется до серной кислоты. Ток электролиза определяется количеством двуокиси серы, подаваемого в единицу времени на поверхность измерительного электрода, и пропорционален концентрации SO2 в газе. Этот ток в достаточно широком интервале не зависит от концентрации серной кислоты и сульфата меди в протекающем растворе, а также не зависит от скорости протекания раствора и анализа руемого газа. [41]
Так как в системе SO-фенол давления оказались относительно небольшими, то был проведен также химический анализ соединения. Затем из трубки откачивали воздух и в нее при - 15 впускали такое количество двуокиси серы, чтобы взятый фенол полностью растворился. [42]
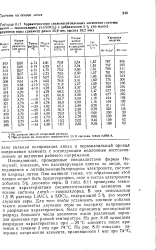 |
Характеристики свежеизготовленных элементов системы литий - тионилхлорид ( Li / SOCl2 с добавлением 5 % ( по массе двуокиси серы ( диаметр равен 25 9 мм, высота 35 2 мм. [43] |
Исследования, проведенные специалистами фирмы Honeywell, показали, что пассивирующая пленка на аноде, находящемся в литийалюминийхлоридном электролите, состоит из хлорида лития. Они выявили также, что образование этой пленки может быть предотвращено, если в состав электролита добавить 5 % двуокиси серы. В табл. 8.11 приведены технические характеристики свежеизготовленных элементов на основе системы литий - тионилхлорид. В них использован 1 5 М раствор ЫА1С14 в SOCh, содержащий 5 % ( по массе) двуокиси серы. Для того чтобы установить влияние добавки такого количества двуокиси серы на задержку напряжения и разрядные характеристики, были проведены исследования разряда большого числа элементов после различных периодов хранения при разной температуре. На рис. 8.40 приведена разрядная характеристика при - 29 С элемента после хранения в течение 2 нед при 74 С. [44]
Так как дитионат разлагается до сульфата, а сульфит окисляется содержащимся в газе кислородом ( или кислородом воздуха), то в результате получается раствор сульфата марганца. Однако манганитные руды реагируют с сернистым газом значительно медленнее пиролюзитных. Увеличение дисперсности ускоряет процесс, лимитируемый, по-видимому, растворением руды, причем содержание в растворе дитионата увеличивается, а сульфата относительно уменьшается. Это объясняется разностью в скоростях растворения руды и разложения дитионата. В отличие от пиролш-зитной руды при разбавлении суспензии из манганитной руды ( от Т: Ж 1: 2 до 1: 10) степень извлечения марганца увеличивается за счет роста количества растворенной двуокиси серы. Повышение концентрации SO2 в газе и в растворе ускоряет разложение дитионата. При обработке водной суспензии манганитной руды ( Т: Ж 1: 10) сернистым газом ( 16 2 - 17 6 % SO2) при избыточном отношении Mn: SOa, равном 1: 1 9, и температуре 80 в течение 3 ч достигается 90 % - ное извлечение марганца в раствор. [45]
Страницы: 1 2 3 4